背景
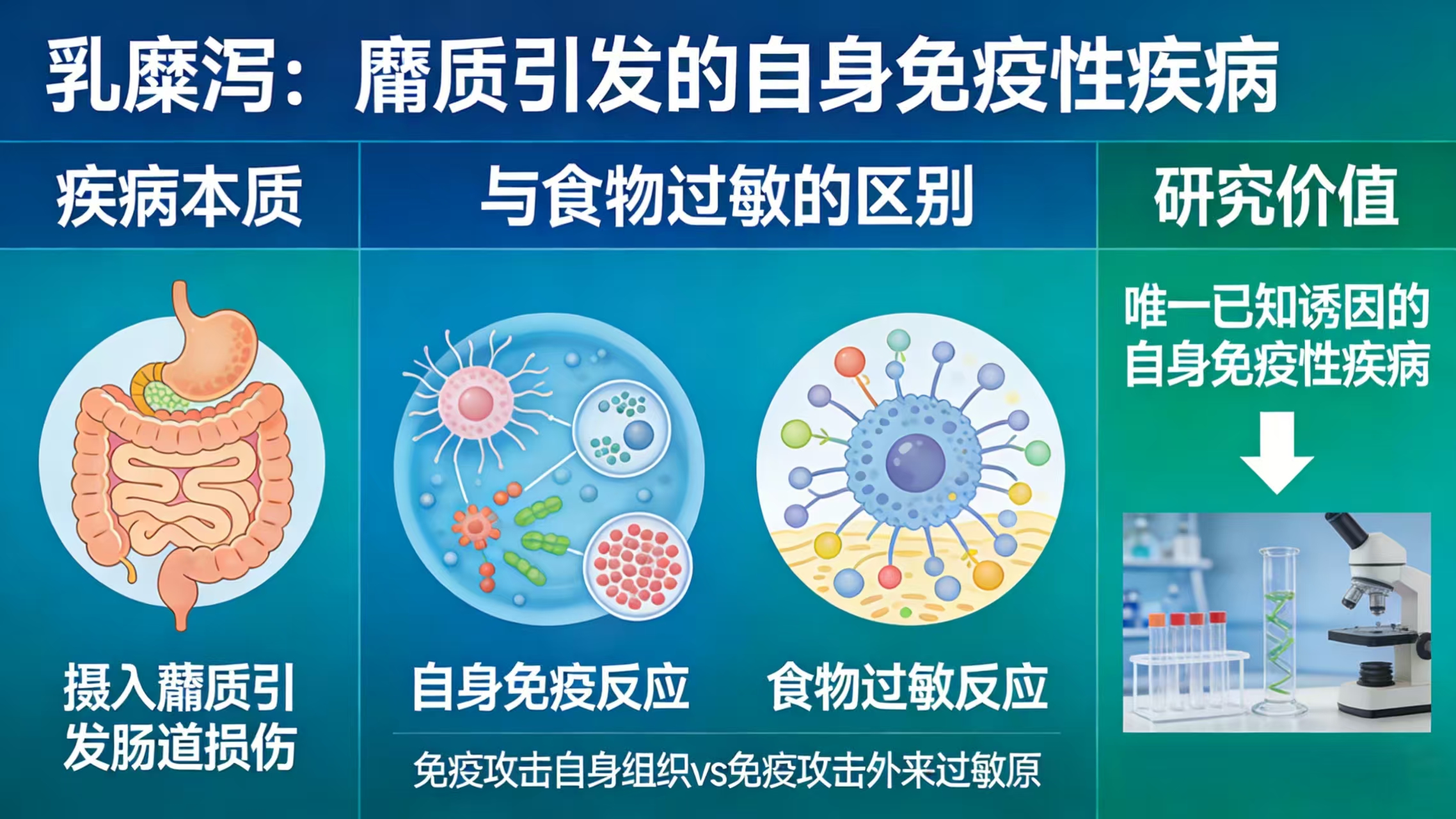
乳糜泻是一种由摄入麸质引发的肠道疾病,且属于自身免疫性疾病(会损害身体自身组织),并非食物过敏,其对麸质的免疫反应与食物过敏机制不同,同时它也是唯一已知诱因的自身免疫性疾病,这一特征为疾病的靶向干预研究提供了关键的切入点。
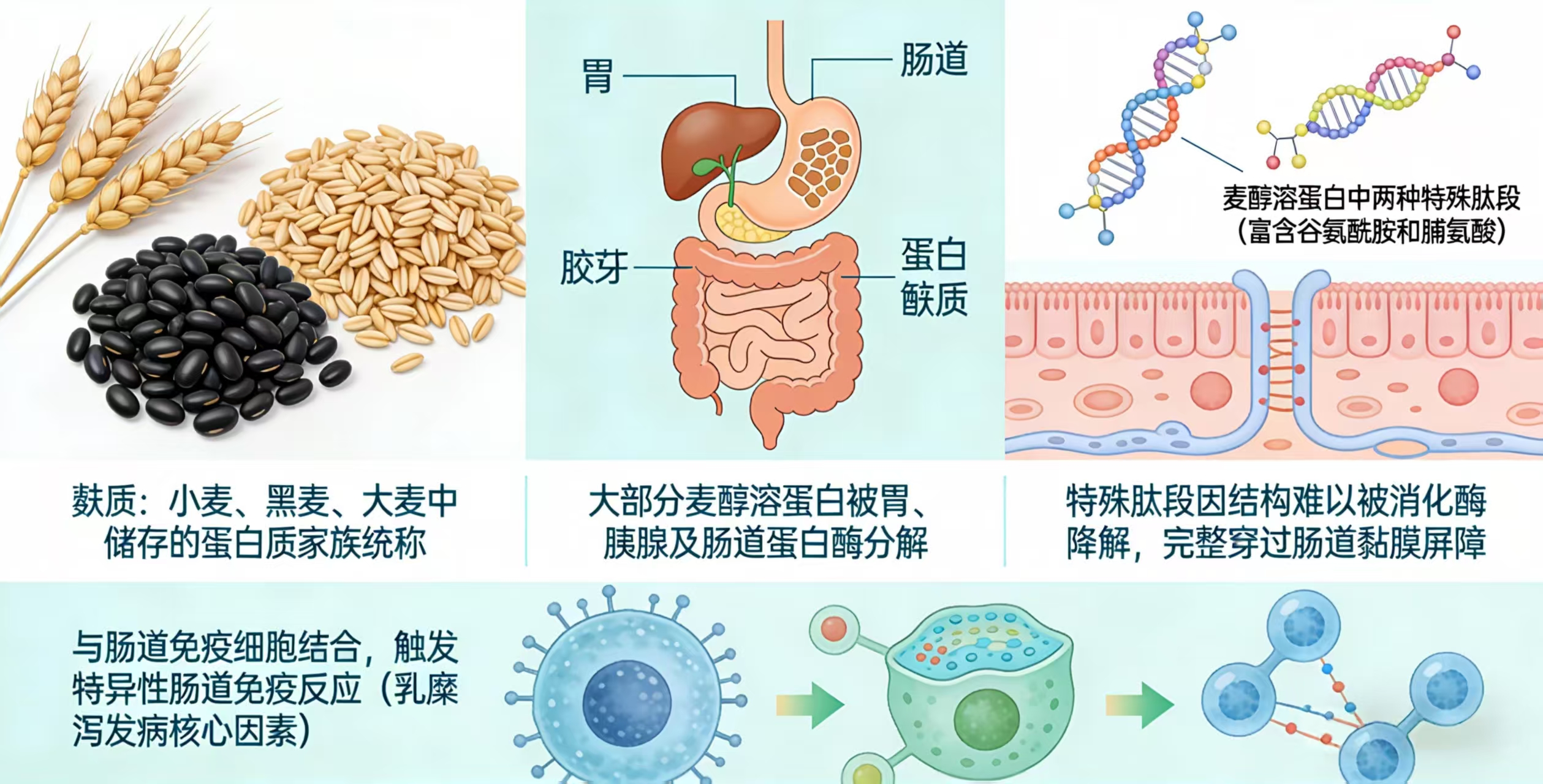
麸质是存在于小麦、黑麦、大麦中储存的蛋白质家族统称,麸质中的麦醇溶蛋白(Gliadin)是主要致病组分,但大部分麦醇溶蛋白会被胃、胰腺及肠道蛋白酶分解;麦醇溶蛋白中存在两种特殊的肽段,因分子结构中高度富含谷氨酰胺和脯氨酸,这类氨基酸的特殊结构使其难以被人体常规的消化酶识别并降解,两种肽段因富含谷氨酰胺和脯氨酸,这类氨基酸的特殊结构使其难以被人体常规的消化酶识别并降解,能够完整穿过肠道黏膜屏障进入体内循环,最终与肠道免疫细胞结合,触发特异性的肠道免疫反应,成为乳糜泻发病的核心关键因素。
引发乳糜泻免疫反应的关键物质是麦醇溶蛋白中抵抗消化的特定肽段,其中:1、33聚体肽(P55-87)主导适应性免疫反应(T细胞依赖);2、P31-43肽段主导固有免疫反应和细胞应激/增殖,是早期黏膜损伤的核心触发物。
目前临床上对于乳糜泻的治疗和长期管理,仍以严格的终身无麸质饮食为核心原则,这也是现阶段全球医学界公认的唯一能从根本上控制病情进展、缓解临床症状的治疗方法。乳糜泻患者需要在日常生活中彻底规避所有含有小麦、黑麦、大麦等麸质原始来源的食物,同时还需要高度警惕各类 “隐藏麸质” 的潜在暴露风险,这类隐藏麸质并非以直观的谷物形式存在,而是常隐匿于食用化制淀粉、加工食品添加剂、调味酱料、代餐制品甚至部分药品的辅料中,稍有不慎的微量摄入就可能引发患者病情反复,给患者的日常饮食管理带来了极高的要求和极大的生活不便。
目标
本研究的核心目标是从乳糜泻的致病机制出发,通过阻断机体免疫系统对麸质致病肽段的识别过程,从源头减少甚至避免异常免疫反应的发生,为乳糜泻患者提供全新的靶向干预手段。研究拟定利用益生菌的生物合成特性,使其产生具有特异性结合能力的肽 “帽”,该肽帽能够与麦醇溶蛋白中的致病性片段进行精准、高效的特异性结合,通过物理遮盖的方式掩盖致病肽段上的免疫识别位点,使机体的免疫系统无法识别并结合这些致病片段,从而彻底防止异常免疫反应的触发,实现对乳糜泻的靶向干预。
乳糜泻的致病根源是麸质中麦醇溶蛋白的 33 聚体肽(P5587,主导适应性免疫)与 P3143 肽段(主导固有免疫)抵抗消化酶降解,触发肠道免疫损伤。目前已有实验证实:黑曲霉脯氨酸内肽酶(AnPEP)可在体外及初步动物模型中切割麸质脯氨酸残基,将部分致病肽段降解为小分子片段(如复杂餐食环境中,AnPEP 对麸质的降解率可达 60% 以上)10;但实验同时发现,受肠道消化酶活性差异、麸质暴露剂量波动(如交叉污染)影响,仍有 15%-20% 的免疫毒性片段(尤其是 33 聚体肽)无法被完全降解,这些残留片段仍可与肠道免疫细胞结合,引发潜在炎症反应。
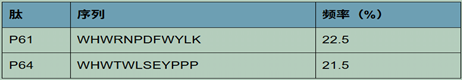
鉴于现有 “酶讲解毒策略无法实现 100% 清除麸质致病肽段” 的核心局限,且 33 聚体肽作为免疫毒性最强的残留片段,是乳糜泻病情反复的关键诱因,本研究团队将后续的研究重心精准聚焦于 P61/P64 肽帽的优化设计上。前期研究已通过大量的体外结合实验,获得了 P61、P64 肽帽的核心氨基酸序列及对应的结合频率数据,其中 P61 肽的氨基酸序列为 WHWRNPDFWYLK,结合频率达 22.5%,P64 肽的氨基酸序列为 WHWTWLSEYPPP,结合频率为 21.5%,而肽帽的观测频率数值能够直接反映其对胶粘蛋白以及麸质免疫优势区的结合特异性和亲和力,二者较高的结合频率为后续的优化设计和功能研究奠定了坚实且可靠的实验基础。
基于 P61/P64 肽帽与胶连蛋白、麸质免疫优势区的天然强亲和力,本研究拟定设计针对乳糜泻致病肽段的 “竞争性结合剂”,该结合剂的整体设计思路围绕 “精准靶向肠道病变部位、高效占据免疫结合位点、稳定阻断致病相互作用” 三大核心原则展开,同时从肠道靶向递送优化、作用机制科学验证、体内外效果全面评估三个关键方面,构建一套完整且系统的乳糜泻靶向干预研究方案,形成从分子设计到效果验证的全流程研究体系,具体的技术路径与验证方法如下:.
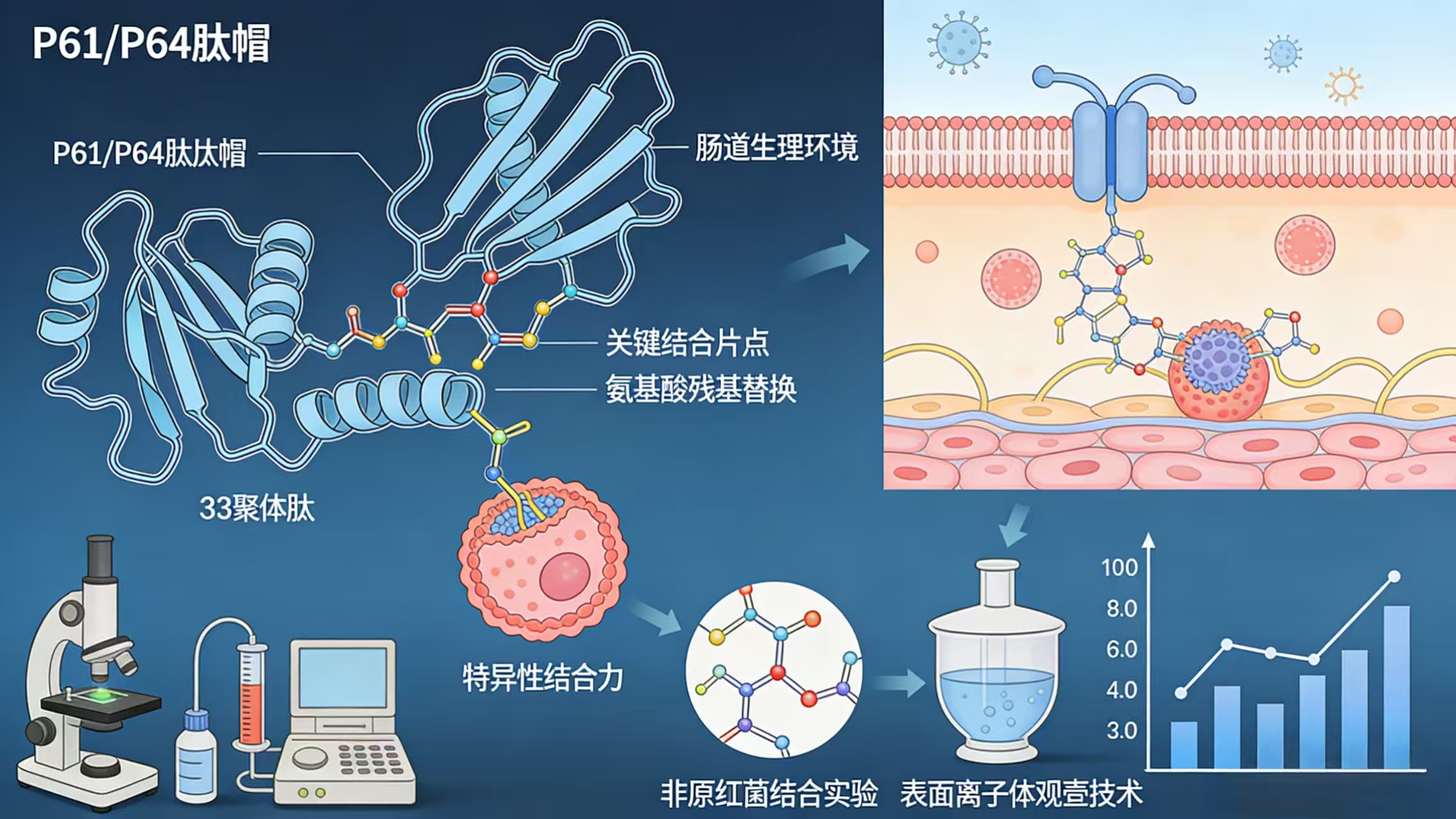
技术路径
本研究将对 P61/P64 肽帽的核心氨基酸序列进行精准的定点微调,通过对关键结合位点的氨基酸残基进行替换、修饰等分子改造手段,进一步增强肽帽与麸质致病片段的特异性结合力,确保优化后的肽帽在肠道复杂的生理环境中,能够凭借更高的结合效率,优先于肠道免疫细胞与致病片段完成结合,从源头阻断免疫识别与结合的关键过程。同时,本研究将通过一系列严谨的体外结合实验验证肽帽的结合专一性,利用抗原抗体结合实验、表面等离子体共振技术、分子对接模拟等多种实验手段,明确优化后的肽帽仅靶向结合致病的 33 聚体肽,避免其与肠道内其他正常的蛋白质、肽段发生非特异性结合,防止对肠道正常的生理功能和免疫平衡造成不必要的干扰。[4].
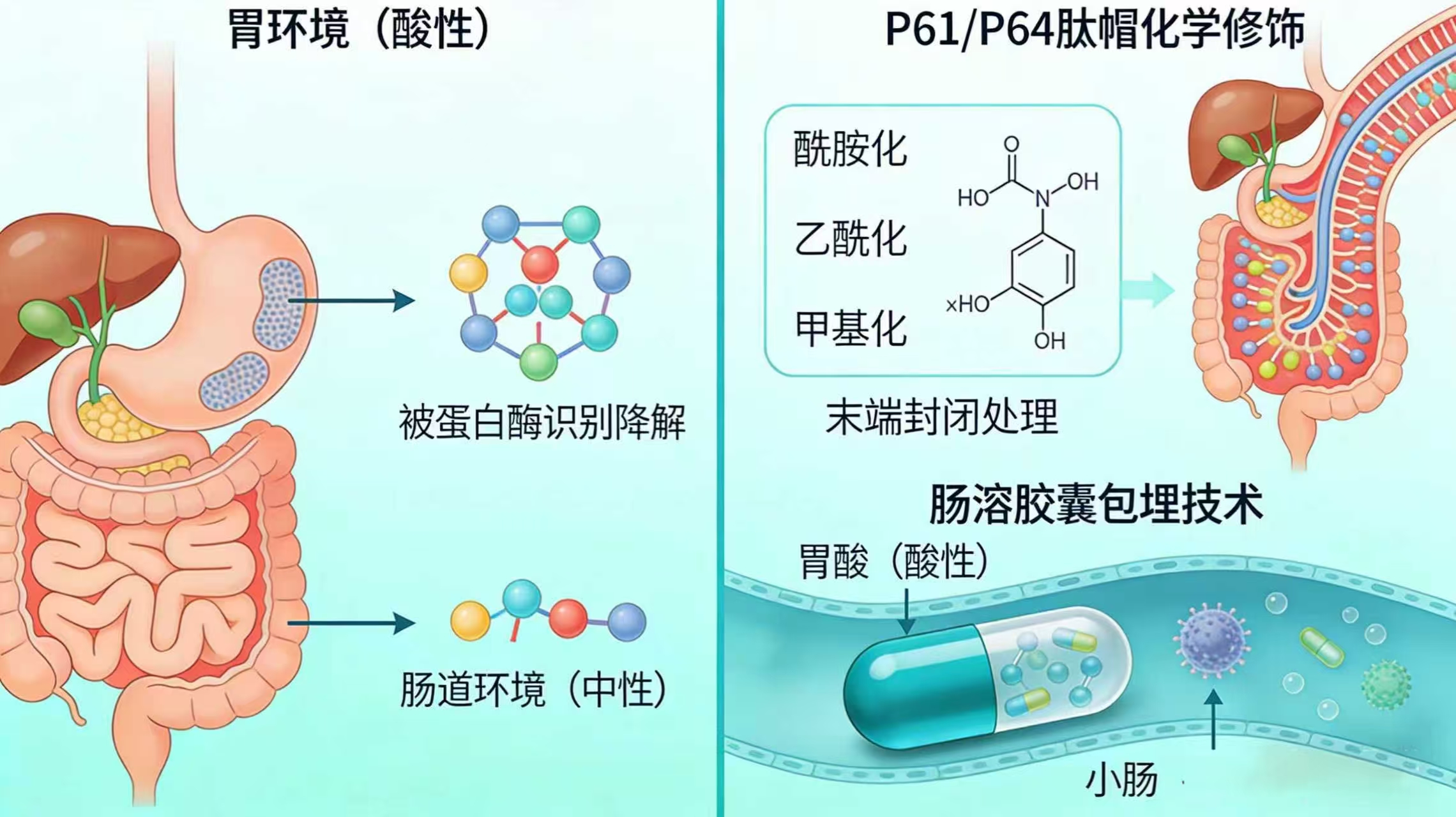
肽类物质在人体消化道内的生物稳定性较差,极易被胃、肠道中的蛋白酶降解,从而失去原有的生物活性,因此本研究将对 P61/P64 肽帽进行针对性的化学修饰和末端封闭处理。通过酰胺化、乙酰化、甲基化等成熟的化学修饰手段,改变肽帽的分子表面结构,保护其关键的肽键不被胃、肠道中的蛋白酶识别并分解,大幅提升肽帽在人体消化道内的生物稳定性。同时,本研究将采用肠溶胶囊包埋技术对优化后的肽帽进行包埋处理,利用肠溶材料的 pH 值敏感性,使包埋肽帽的胶囊在胃酸的酸性环境中保持结构稳定、不溶解,仅在小肠部位 —— 乳糜泻发病的核心病理区域,pH 值呈弱碱性的环境中精准释放肽帽活性成分,有效避免胃酸对肽帽的破坏,确保活性成分能够顺利抵达肠道的关键作用位点。
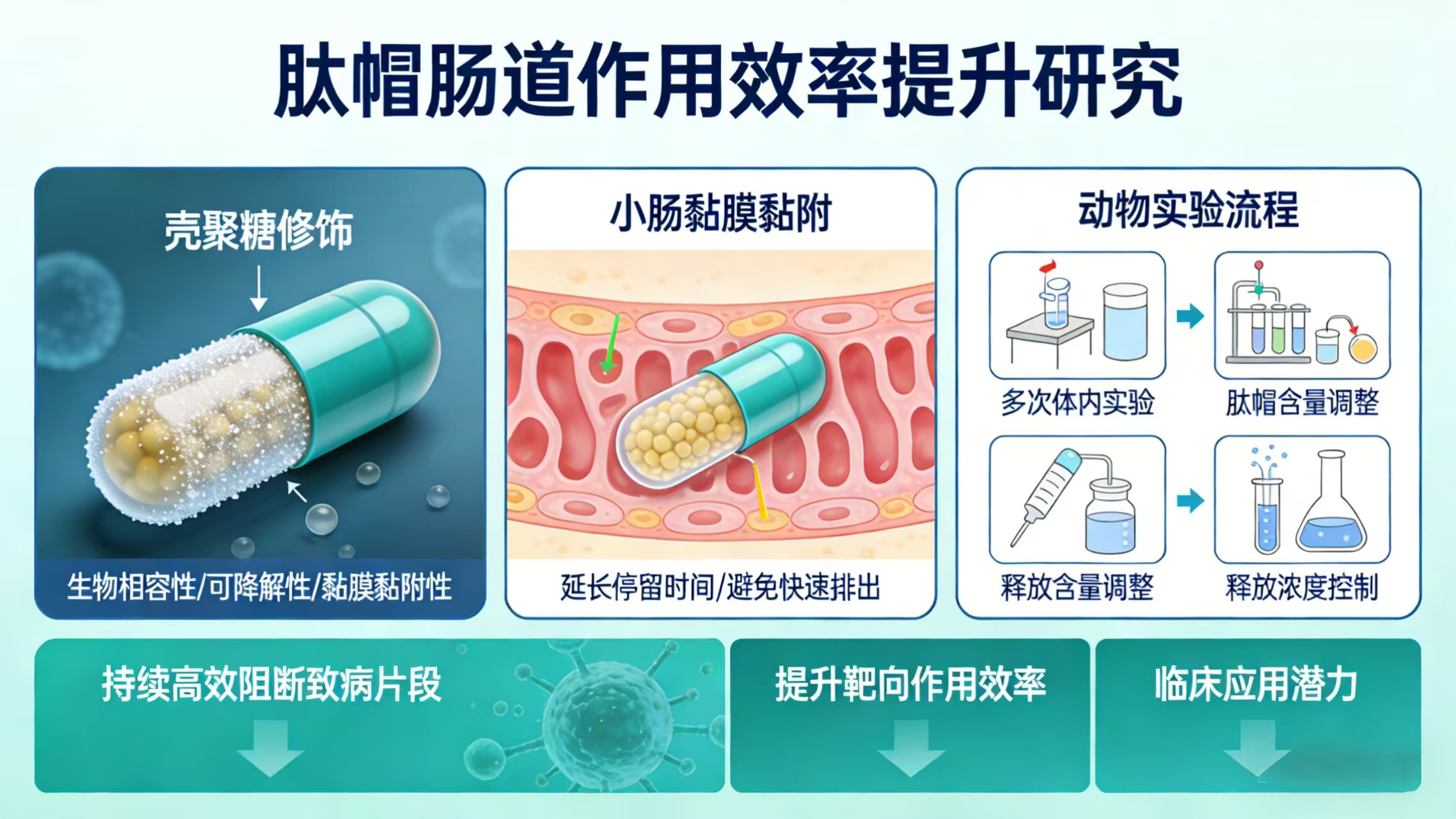
为进一步提升肽帽在肠道内的作用效率和持续时间,本研究将在肠溶胶囊的表面进行壳聚糖修饰处理。壳聚糖是一种具有良好生物相容性、生物可降解性和黏膜黏附性的天然多糖,经壳聚糖修饰后的肠溶胶囊能够紧密黏附于小肠黏膜表面,有效延长肽帽在小肠内的停留时间,避免其随肠道的正常蠕动快速排出体外。同时,本研究将通过多次体内动物实验,反复摸索并精准调整胶囊内肽帽的有效含量,实现对肽帽在小肠内释放浓度的精准控制,保证肠道内始终维持能够有效阻断致病片段的肽帽浓度,实现对残留致病片段的持续、高效阻断,大幅提升肽帽的靶向作用效率和临床应用潜力。
单一的阻断策略在应对复杂的人体肠道环境时仍存在一定的局限性,因此本研究将采用协同干预的思路,将优化后的肽帽与能够稳定表达 AnPEP 的 EcN 益生菌进行共包埋处理,将二者共同封装于肠溶微囊中,实现 “酶讲解毒 + 肽帽阻断” 的同步协同作用。在人体肠道的生理环境中,肠溶微囊会精准释放 EcN 益生菌和肽帽,其中 EcN 益生菌会率先分泌黑曲霉脯氨酸内肽酶,对摄入肠道的麸质进行高效的酶解降解,将大部分麸质致病肽段分解为无免疫毒性的小分子片段;对于剩余未被酶解的残留致病片段,则由同时释放的优化肽帽进行精准的特异性结合、物理阻断,有效避免因酶解与阻断作用不同步导致的致病片段 “漏网”,通过二者的协同互补作用,实现对麸质致病肽段的全方位、多层次干预,大幅提升整体的免疫阻断效果。
验证与未来发展方向
验证肽帽能够有效结合并遮盖致病片段:本研究采用荧光标记技术对麸质致病片段进行特异性荧光标记,将标记后的致病片段与优化后的肽帽在模拟人体肠道的生理环境中进行混合培养,通过荧光显微镜和流式细胞术等检测手段观察免疫细胞对标记片段的识别情况。实验结果清晰显示,免疫细胞几乎无法识别到荧光标记的致病片段,这一结果充分表明优化后的肽帽能够与致病片段实现精准、高效的特异性结合,成功盖住致病片段上的免疫识别关键位置,使机体的免疫系统无法对其进行识别和结合。
验证肽帽能够有效抑制异常免疫反应:本研究通过体外细胞培养技术,构建肠道上皮细胞与免疫细胞的共培养模型,高度模拟人体肠道的免疫微环境,向该模型中同时加入麸质致病片段及优化后的肽帽,设置未加入肽帽的空白对照组进行对比。通过检测免疫细胞的活化程度、炎症相关细胞因子的分泌水平等指标,发现与空白对照组相比,加入肽帽的实验组中免疫细胞的活跃度出现明显降低,同时肠道内引发炎症的细胞因子、炎症介质等物质的分泌量也大幅减少,这表明肽帽能够有效阻断免疫反应的整个传导过程,从根本上抑制机体针对麸质的异常免疫炎症的发生和发展。
验证肽帽能够有效保护肠道屏障完整性:本研究通过体外肠道黏膜模型实验,专门验证麸质致病片段及肽帽对肠道屏障结构和功能的影响。实验结果发现,单纯的麸质致病片段会显著破坏肠道黏膜的紧密连接结构,损伤肠道的天然 “保护层”,导致肠道屏障的通透性大幅增加,引发肠道内物质的异常渗漏;而在同时加入优化肽帽后,肠道黏膜的紧密连接结构能够保持完整,肠道的天然 “保护层” 基本未受到损伤,肠道黏膜的通透性也维持在正常的生理水平,这表明肽帽能够通过阻断致病片段与免疫细胞的结合,从源头减少免疫反应对肠道屏障的损伤,同时间接保护肠道屏障的结构和功能完整性,进一步降低异常免疫反应的发生概率。
肽帽序列迭代优化:本研究将借助 AlphaFold 人工智能蛋白结构预测技术,结合 X 射线晶体衍射、冷冻电镜等实验手段,精准解析 33 聚体肽的三维空间结构,明确其分子表面的多个免疫表位的具体分布特征和结合位点。以此为核心研究基础,开展大规模的高通量筛选实验,将噬菌体展示文库的库容量扩容至 10¹²,通过大规模、高效率的筛选工作,寻找能够对 33 聚体肽多个免疫表位均具有高亲和力的 “多价肽帽”,突破现有肽帽单一位点结合的局限性,进一步提升肽帽的免疫阻断广谱性和结合效率,实现对 33 聚体肽的全方位、多靶点结合阻断,大幅增强肽帽的干预效果。
剂型升级:在现有肠溶胶囊剂型的基础上,本研究将开发全新的 “口服凝胶剂” 剂型。该口服凝胶剂将选用具有良好黏膜粘附性、成膜性和生物相容性的天然高分子材料作为基质,患者口服后,凝胶剂能够在口腔、食道黏膜表面快速形成一层均匀、致密的保护膜,提前结合饮食过程中可能存在的微量麸质,从消化道的上游环节减少麸质进入肠道的剂量,降低后续肠道的麸质暴露量。该剂型将与小肠内发挥作用的肽帽肠溶胶囊形成 “上游拦截 + 下游阻断
人群初步验证:本研究将开展小规模的人体初步验证实验,严格按照临床研究的规范要求,选取 20-30 例经肠镜和血清学检查确诊的乳糜泻患者作为研究对象,在患者坚持严格无麸质饮食的基础上,让其规律、定量补充优化后的 P61/P64 肠溶微囊。通过为期 3 个月的持续跟踪监测,定期检测患者的血清炎症因子水平、营养吸收相关指标(如血清白蛋白、维生素 B 族、铁、锌等矿物质),同时详细记录患者的主观临床症状(如腹痛、腹泻、腹胀、消化不良等)的改善情况和发作频率,全面、系统地验证 P61/P64 肽帽在人体中的免疫阻断效果、生物安全性和耐受性,为后续开展大规模的临床研究、推动肽帽的临床转化和实际应用提供关键的人体实验数据支持。
参考文献
[1] Fasano, A. Systemic autoimmune disorders in celiac disease. Current opinion in gastroenterology 22, 674-679, doi:10.1097/01.mog.0000245543.72537.9e (2006).
[2] Sapone, A. et al. Spectrum of gluten-related disorders: consensus on new nomenclature and classification. BMC medicine 10, 13, doi:10.1186/1741-7015-10-13 (2012).
[3] López Casado, M. Á., Lorite, P., Ponce de León, C., Palomeque, T. & Torres, M. I. Celiac Disease Autoimmunity. doi:10.1007/s00005-018-0520-z (2018).
[4] Koehler, P. & Wieser, H. J. G. p. Structure and functionality of gluten proteins: An overview. 84-88 (2009).
[5] Londei, M. et al. Gliadin as a stimulator of innate responses in celiac disease. 42, 913-918 (2005).
[6] Morón, B. et al. Sensitive detection of cereal fractions that are toxic to celiac disease patients by using monoclonal antibodies to a main immunogenic wheat peptide. 87, 405-414 (2008).
[7]Sollid, L. M. & Jabri, B. Triggers and drivers of autoimmunity: lessons from coeliac disease. Nature reviews. Immunology 13, 294-302, doi:10.1038/nri3407 (2013).
[8]Discepolo, V., Kelly, C. P., Koning, F. & Schuppan, D. How Future Pharmacologic Therapies for Celiac Disease Will Complement the Gluten-Free Diet. Gastroenterology 167, 90-103, doi:10.1053/j.gastro.2024.02.050 (2024).
[9]Blom, J. J., Gidrewicz, D., Turner, J., Duerksen, D. R. & Pinto-Sánchez, M. I. Diagnosis and management of celiac disease. CMAJ : Canadian Medical Association journal = journal de l'Association medicale canadienne 197, E1258-e1265, doi:10.1503/cmaj.230091 (2025).
[10]König, J., Holster, S., Bruins, M. J. & Brummer, R. J. Randomized clinical trial: Effective gluten degradation by Aspergillus niger-derived enzyme in a complex meal setting. Scientific reports 7, 13100, doi:10.1038/s41598-017-13587-7 (2017).
