工程循环
四个工程周期 · 从设计到学习的闭环迭代
循环1 · 菌株选择
研究
想象
设计与构建
测试
学习
循环2 · 感知灵敏度
研究
想象
设计与构建
测试
学习
循环3 · 三联疗法
研究
IFN-ω针对病毒诱因,从源头减少病毒触发;LL-37控制细菌继发感染,恢复口腔菌群平衡;TGF-β1调节免疫紊乱,从根本上抑制过度炎症反应。三者联用可实现对猫口炎“病毒-细菌-免疫”三大病因的协同治疗,弥补现有单一疗法的不足。因此,我们选择IFN-ω、LL-37、TGF-β1作为三联疗法的核心治疗蛋白。
想象
设计与构建
pSB1C3-FeloVance 质粒图谱
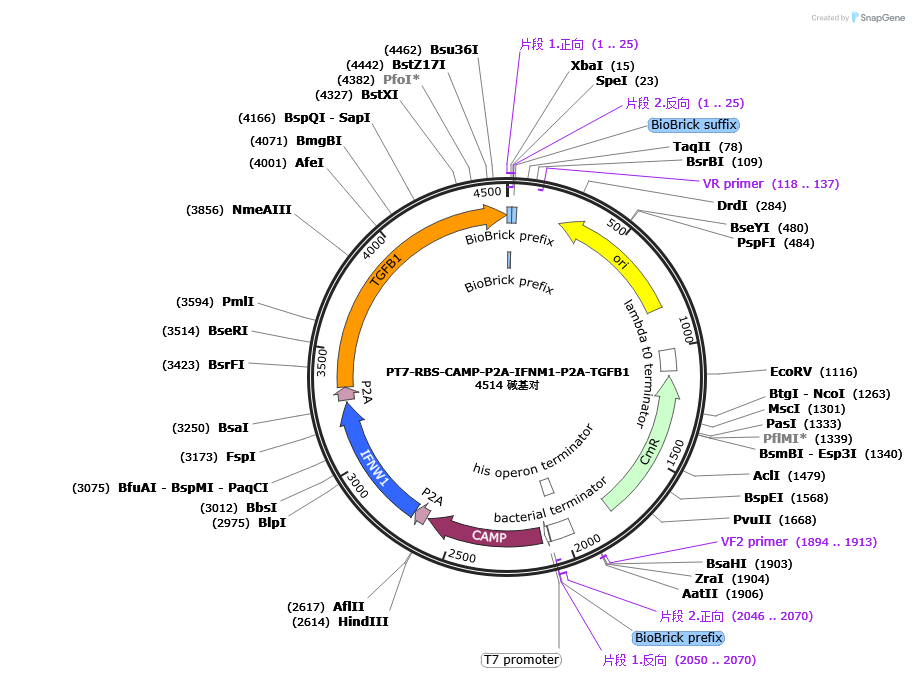
图:pSB1C3-FeloVance 三联疗法表达质粒 · 包含 T7启动子、RBS、IFN-ω、P2A、LL-37、P2A、TGF-β1、终止子
测试
学习
循环4 · 安全性设计
研究
想象
设计与构建
测试
学习
参考文献
[1]Effendi SSW, Ng IS. Innovations, Challenges and Future Directions of T7RNA Polymerase in Microbial Cell Factories. ACS Synth Biol. 2025 May 16;14(5):1381-1396. doi: 10.1021/acssynbio.5c00139. Epub 2025 Apr 10. PMID: 40209062; PMCID: PMC12090346.
[2]Vandamme D, Landuyt B, Luyten W, Schoofs L. A comprehensive summary of LL-37, the factotum human cathelicidin peptide. Cell Immunol. 2012 Nov;280(1):22-35. doi: 10.1016/j.cellimm.2012.11.009. Epub 2012 Nov 29. PMID: 23246832.
[3]Kaci G, Goudercourt D, Dennin V, Pot B, Doré J, Ehrlich SD, Renault P, Blottière HM, Daniel C, Delorme C. Anti-inflammatory properties of Streptococcus salivarius, a commensal bacterium of the oral cavity and digestive tract. Appl Environ Microbiol. 2014 Feb;80(3):928-34. doi: 10.1128/AEM.03133-13. Epub 2013 Nov 22. PMID: 24271166; PMCID: PMC3911234.
[4]Liu Z, Chen O, Wall JBJ, Zheng M, Zhou Y, Wang L, Vaseghi HR, Qian L, Liu J. Systematic comparison of 2A peptides for cloning multi-genes in a polycistronic vector. Sci Rep. 2017 May 19;7(1):2193. doi: 10.1038/s41598-017-02460-2. PMID: 28526819; PMCID: PMC5438344.
[5]Wang X, Li F, Han M, Jia S, Wang L, Qiao X, Jiang Y, Cui W, Tang L, Li Y, Xu YG. Cloning, Prokaryotic Soluble Expression, and Analysis of Antiviral Activity of Two Novel Feline IFN-ω Proteins. Viruses. 2020 Mar 19;12(3):335. doi: 10.3390/v12030335. PMID: 32204464; PMCID: PMC7150924.
[6]Stewart AG, Thomas B, Koff J. TGF-β: Master regulator of inflammation and fibrosis. Respirology. 2018 Dec;23(12):1096-1097. doi: 10.1111/resp.13415. Epub 2018 Oct 4. PMID: 30284753.
[7]Stirling F, Naydich A, Bramante J, Barocio R, Certo M, Wellington H, Redfield E, O'Keefe S, Gao S, Cusolito A, Way J, Silver P. Synthetic Cassettes for pH-Mediated Sensing, Counting, and Containment. Cell Rep. 2020 Mar 3;30(9):3139-3148.e4. doi: 10.1016/j.celrep.2020.02.033. PMID: 32130913.
[8]Stirling F, Bitzan L, O'Keefe S, Redfield E, Oliver JWK, Way J, Silver PA. Rational Design of Evolutionarily Stable Microbial Kill Switches. Mol Cell. 2017 Nov 16;68(4):686-697.e3. doi: 10.1016/j.molcel.2017.10.033. Erratum in: Mol Cell. 2018 Oct 18;72(2):395. doi: 10.1016/j.molcel.2018.10.002. PMID: 29149596; PMCID: PMC5812007.
[9]Uppal S, Akkipeddi VS, Jawali N. Posttranscriptional regulation of cspE in Escherichia coli: involvement of the short 5'-untranslated region. FEMS Microbiol Lett. 2008 Feb;279(1):83-91. doi: 10.1111/j.1574-6968.2007.01009.x. PMID: 18177308.