Overview
烧伤创面的治疗并不是一个静态过程,而是一个随时间持续变化的动态系统。在不同阶段,创面微环境中的关键信号并不相同:烧伤早期通常表现为 pH 升高、ROS 升高,提示炎症和氧化应激增强;若创面发生感染,则会进一步出现病原菌相关信号;而进入愈合后期后,氧气水平升高、MMP-9 下降,则可作为工程菌安全退出的触发条件。
因此,我们的项目并不是一个"持续释放固定药物"的普通敷料,而是一个能够感知环境、切换状态、执行不同功能并最终安全退出的工程菌活体敷料系统。
基于这一设计理念,我们将建模工作分成三个层次:
- 创面微环境输入建模:描述不同场景下的环境信号如何随时间变化;
- 功能模块建模:验证抗炎修复模块与抗铜绿感染模块是否按预期工作;
- 系统级建模:评估状态切换逻辑、kill switch 退出行为,以及整套系统在不同场景下的整体性能。
1. 创面微环境输入模型
1.1 建模目的
后续所有功能模块的激活都依赖于创面微环境,因此我们首先建立了一个创面环境输入模型,将烧伤创面中的关键变量抽象为随时间变化的函数,并在统一框架下比较不同场景。
本模型考虑了六类环境输入:
- 创面 pH
- ROS
- O₂
- MMP-9
- 铜绿假单胞菌感染信号 3-oxo-C12-HSL
- 金黄色葡萄球菌感染信号 Aur
我们统一考虑三种典型场景:
- 无感染烧伤场景
- 铜绿假单胞菌感染场景
- 金黄色葡萄球菌感染场景
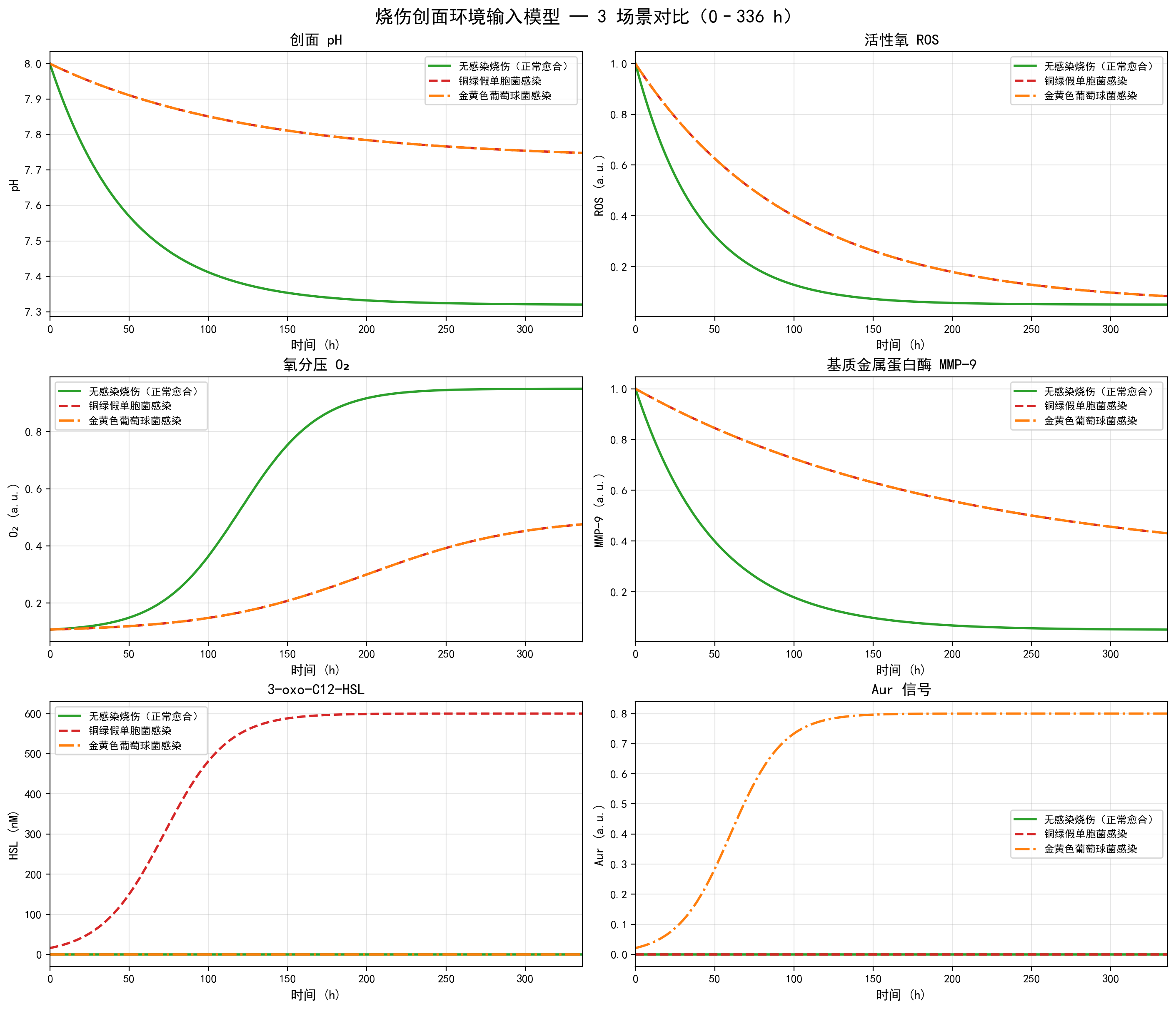
在无感染场景中,pH 和 ROS 在早期较高,随后逐渐下降;氧气水平初期较低,后期逐渐恢复;MMP-9 则在早期较高,后期下降。
在铜绿感染场景中,HSL 随时间上升并维持高位;在金葡感染场景中,Aur 随时间建立并维持高位。
这些输入为后续模块的动态激活提供了统一的时间依赖背景。
为了将烧伤创面环境表示为可计算的动态输入,我们将关键环境变量写成随时间变化的经验函数。对于无感染烧伤场景,我们采用如下形式:
对于感染场景中的病原体信号,我们分别定义:
其中,\(pH(t)\)、\(ROS(t)\)、\(O_2(t)\) 和 \(MMP9(t)\) 描述创面从炎症期到愈合期的环境演化;\(HSL(t)\) 和 \(Aur(t)\) 分别代表铜绿假单胞菌和金黄色葡萄球菌感染信号随时间建立的过程。
2. 双信号抗炎修复模块建模
2.1 建模目的
烧伤创面早期的主要问题是炎症和氧化应激,因此我们首先建立了一个双输入抗炎修复模块模型。该模块被设计为一个 AND gate,要求系统只有在高 pH 与高 ROS 同时存在时,才显著表达 SOD 和 EGF。
这一模块的建模主要回答两个问题:
- 该模块是否在逻辑上满足 AND gate 的设计目标?
- 在连续动态环境中,它是否能够实现"早期激活、后期自动关闭"?
2.2 逻辑层建模
在逻辑层中,我们设定:
- 高 pH 激活上游输入 1;
- 高 ROS 激活上游输入 2;
- 两个输入同时存在时,系统形成有效激活复合体;
- 复合体驱动下游 SOD 和 EGF 表达。
因此,从逻辑上讲,该模块应满足:
| pH | ROS | 输出 |
|---|---|---|
| 高 | 高 | 高 |
| 高 | 低 | 低 |
| 低 | 高 | 低 |
| 低 | 低 | 低 |
这意味着系统只有在烧伤早期典型炎症环境中才会进入修复状态。
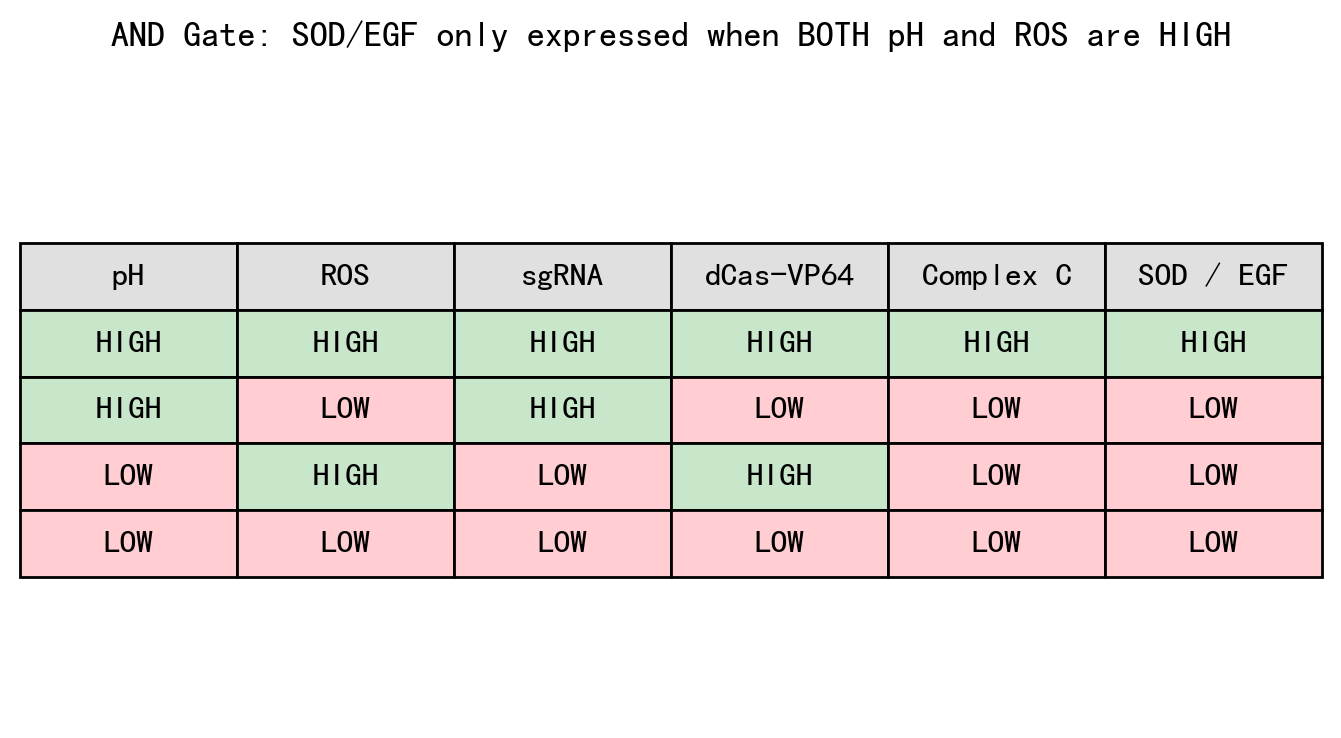
逻辑门表达
我们首先将该模块抽象为一个双输入 AND gate:
其中两个输入采用平滑激活函数表示,而不是硬阈值切换。
输入激活函数
由于 pH 的变化范围较窄,我们使用 sigmoid 形式表示 pH 激活:
ROS 则采用 Hill 函数表示:
模块动力学方程
设 \(g(t)\) 表示 sgRNA,\(d(t)\) 表示 dCas-VP64,\(C(t)\) 表示激活复合体,\(S(t)\) 和 \(E(t)\) 分别表示 SOD 与 EGF,则:
2.3 四条件标准动力学验证
在逻辑层验证之后,我们进一步在四种标准条件下对系统进行动力学模拟:
- High pH + High ROS
- High pH + Low ROS
- Low pH + High ROS
- Low pH + Low ROS
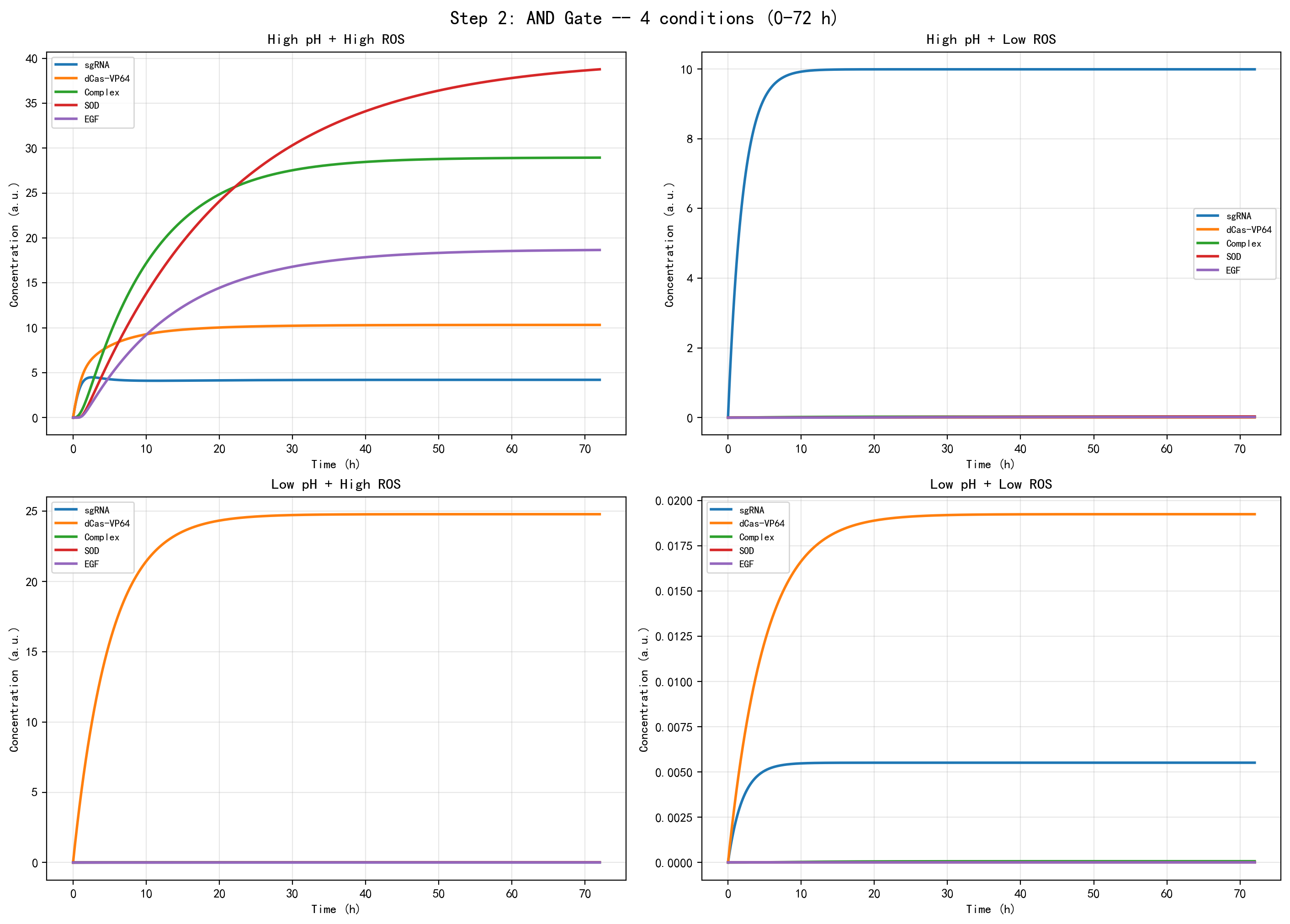
结果表明:
- 仅在 High pH + High ROS 条件下,SOD 和 EGF 输出显著增强;
- 在其余三种条件下,即使某些中间元件存在积累,最终输出仍接近于零。
这说明该模块不仅在布尔逻辑上满足 AND gate,而且在连续动力学层面也具有较好的输入选择性。
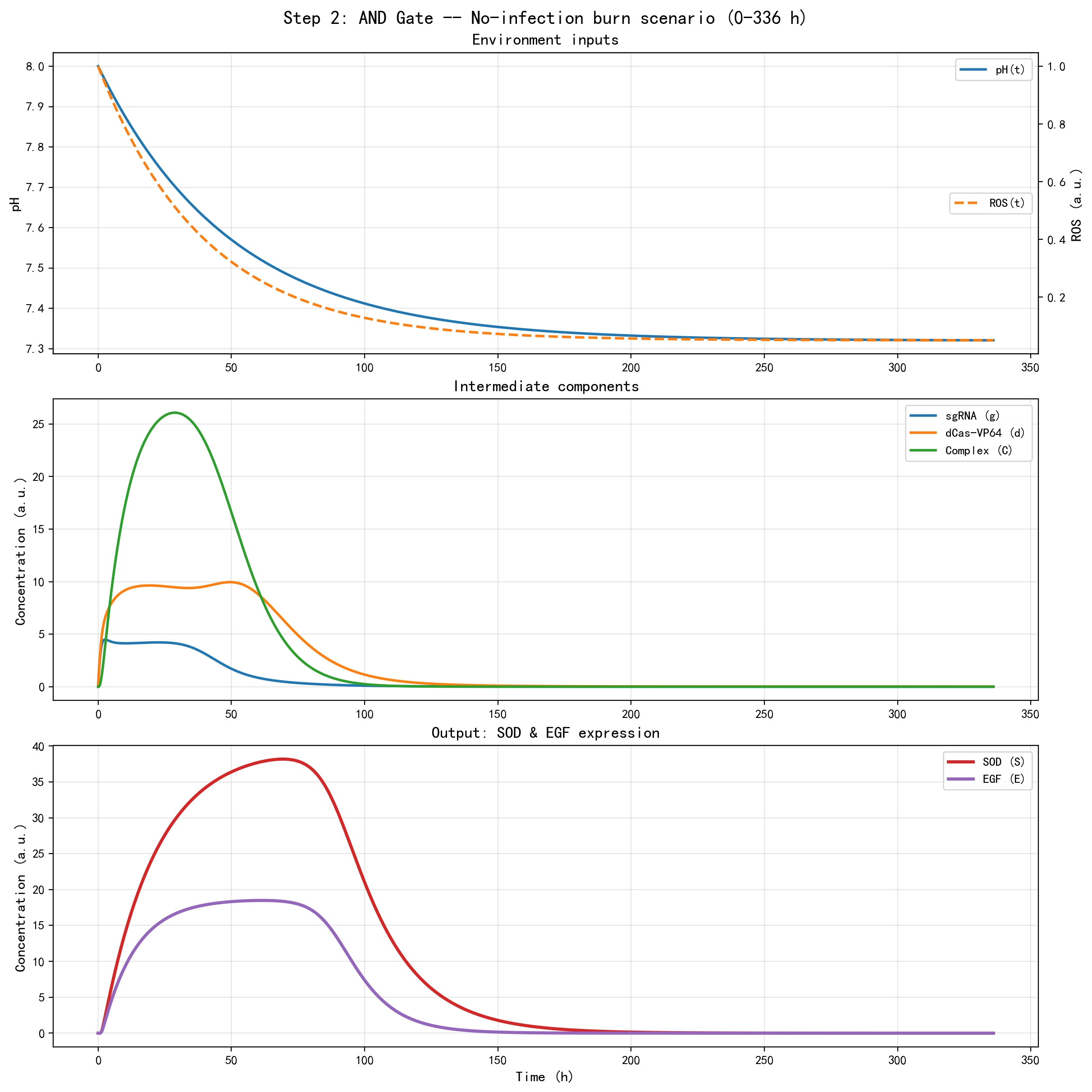
2.4 真实无感染烧伤场景中的动态行为
在无感染烧伤场景中,pH 和 ROS 在创面早期均较高,因此系统能够被迅速激活,产生较强的 SOD 和 EGF 输出。随着创面逐步愈合,pH 和 ROS 下降,系统激活强度随之减弱,最终输出回归基线。
这一结果表明,该模块具有明确的时间窗口:
因此,该模块能够很好地承担"早期抗炎修复"的功能。
3. 铜绿假单胞菌响应模块建模
3.1 建模目的
铜绿假单胞菌是烧伤创面中的重要条件致病菌之一,因此我们建立了一个基于 HSL 信号 的抗感染模块模型,用于模拟系统对铜绿感染的特异性响应。
本模块主要描述以下过程:
- HSL 输入
- 保护模块表达
- Pyocin S5 前体及活性形式建立
- 铜绿菌负荷变化
其核心问题是:
- HSL 是否能够驱动 Pyocin S5 形成浓度依赖响应?
- 在不同 HSL 条件下,模块是否具有明显不同的动态行为?
- 在真实铜绿感染场景下,该模块是否能持续响应?
HSL 剂量-响应函数
我们首先用 Hill 函数描述 HSL 对模块输出的激活作用:
该函数用于刻画 HSL 浓度与 Pyocin S5 表达强度之间的剂量依赖关系。
模块动力学方程
设 \(P_{prot}(t)\) 为保护蛋白,\(P_{pre}(t)\) 为 Pyocin S5 前体,\(P_{act}(t)\) 为活化 Pyocin S5,则:
铜绿菌种群动力学
设 \(B_p(t)\) 表示铜绿假单胞菌负荷,则其增长与杀菌项可写为:
其中 \(\Phi(P_{act})\) 表示由活性 Pyocin S5 介导的杀菌强度,采用饱和函数:
该模型反映了铜绿菌在自身增长与特异性杀伤之间的动态平衡。
3.2 剂量-响应关系
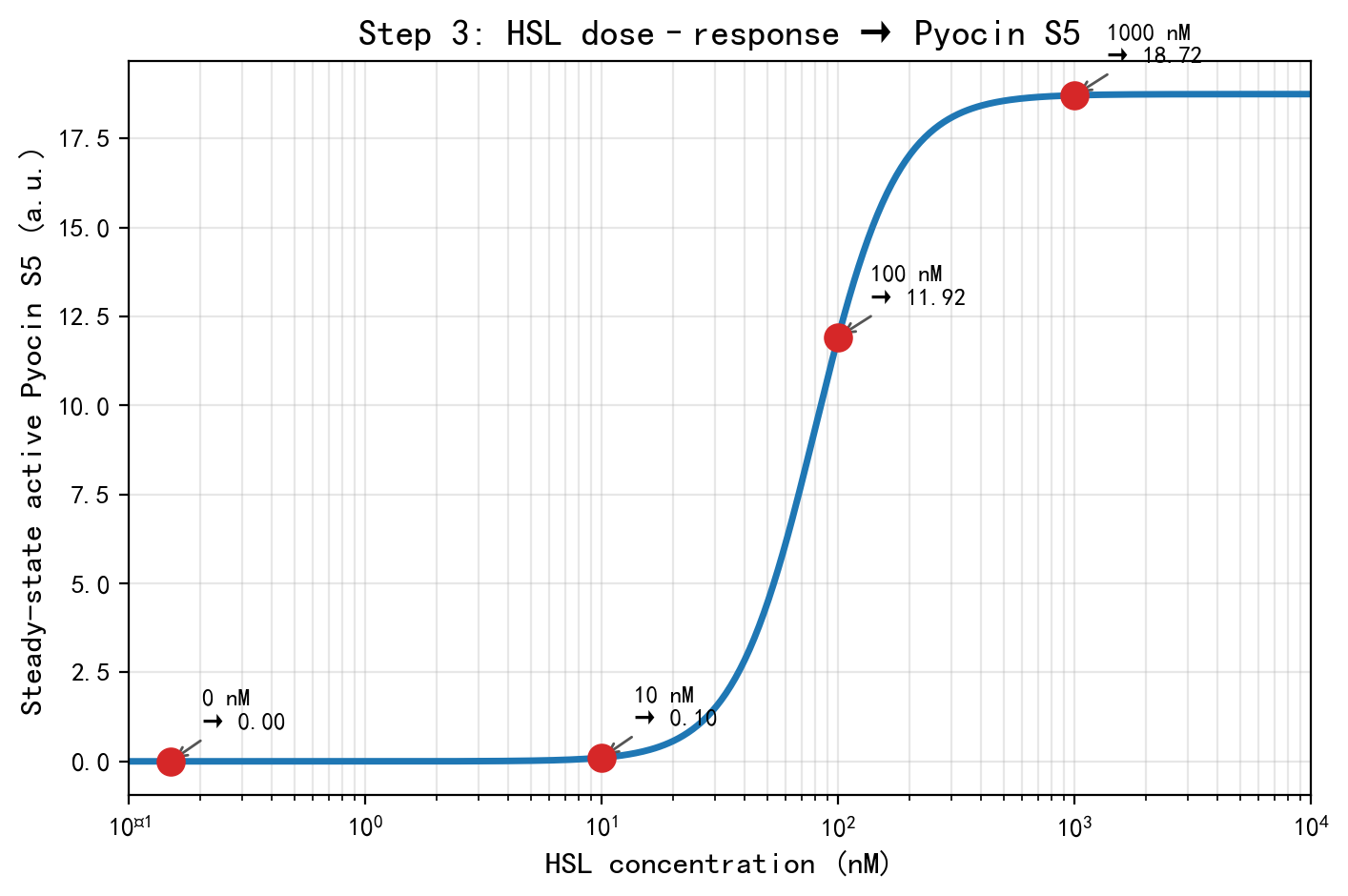
首先,我们建立了 HSL 到活性 Pyocin S5 输出的剂量-响应曲线。
结果显示:
- 在极低 HSL 水平下,Pyocin S5 输出接近于零;
- 随着 HSL 浓度升高,输出迅速增强;
- 在较高浓度范围内,输出逐渐趋于饱和。
这表明铜绿响应模块能够将感染信号的强度连续地映射为功能输出强度,具有明确的剂量依赖特征。
3.3 固定 HSL 条件下的动力学行为
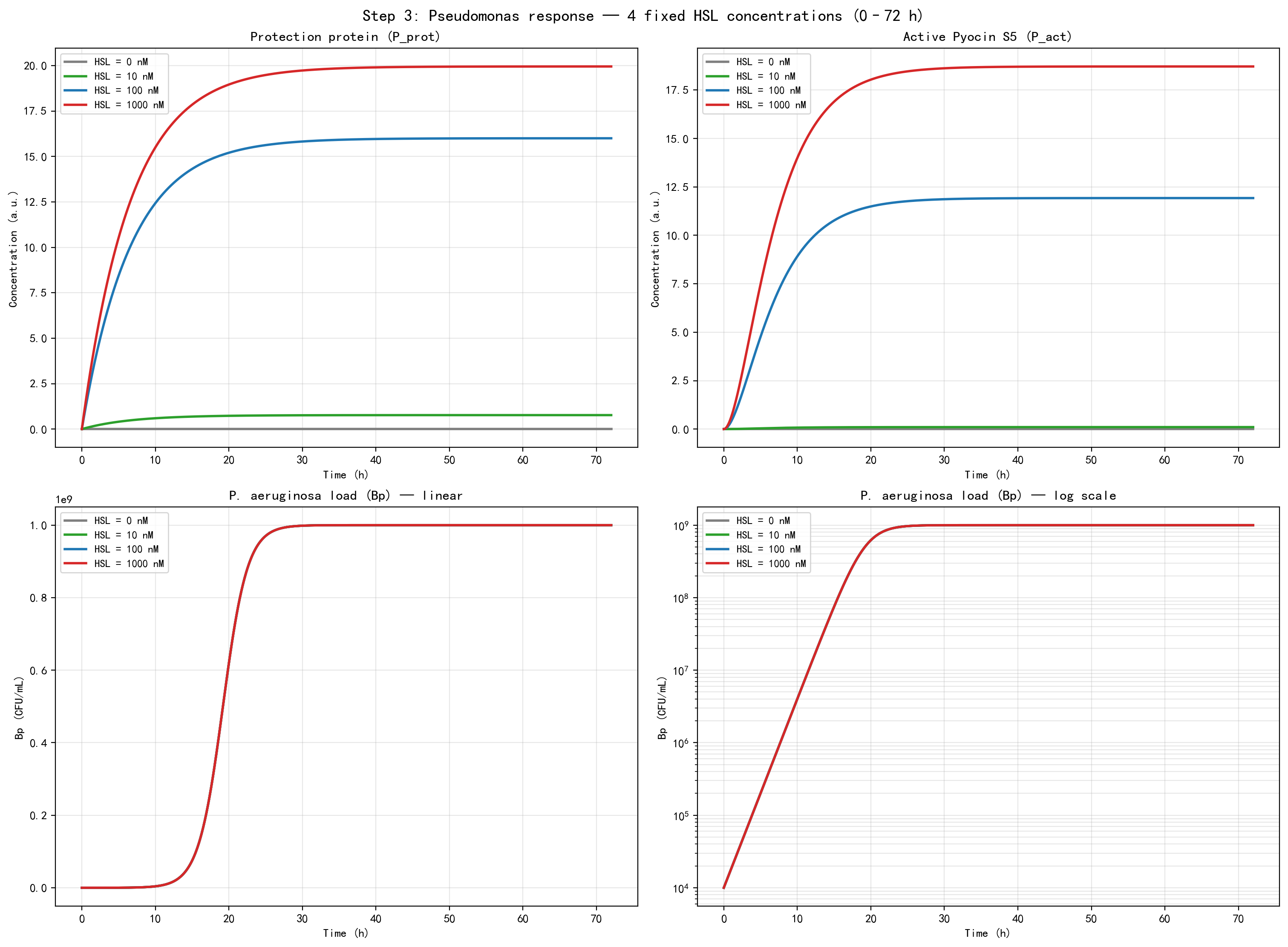
在 0、10、100、1000 nM 四种固定 HSL 条件下,我们分别模拟了:
- 保护蛋白水平
- 活性 Pyocin S5 输出
- 铜绿菌负荷变化
结果表明:
- HSL 越高,保护模块与 Pyocin S5 建立越快、稳态水平越高;
- 不同输入条件下,系统表现出显著不同的输出强度;
- 铜绿菌负荷变化可以随着模块输出而发生差异。
这说明模块能够稳定地将感染输入转化为可持续的动力学响应。
3.4 真实铜绿感染场景中的动态响应
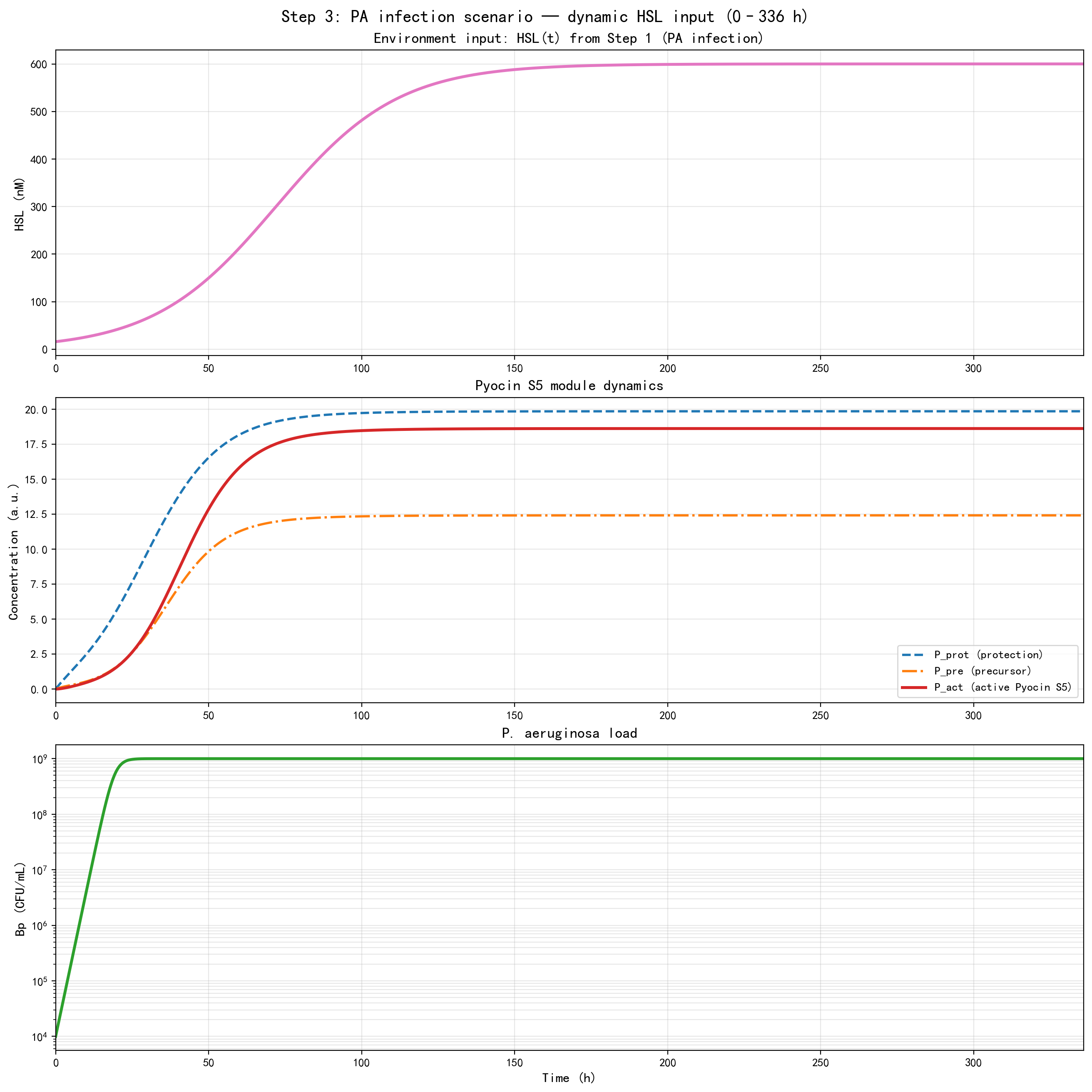
在铜绿感染烧伤场景中,HSL 随时间逐步升高。模型结果显示,随着 HSL 信号建立:
- 保护模块逐渐增强;
- 活性 Pyocin S5 输出持续升高;
- 模块进入稳定的抗感染工作状态。
这说明铜绿响应模块并不是对瞬时信号做出短暂反应,而是能够在真实感染背景下形成持续的响应过程。
4. 状态切换模型
4.1 建模目的
前述模块分别解决了"单个模块能否工作"的问题,但对于一个真正的活体敷料系统而言,还必须进一步回答:
因此,我们建立了一个系统级状态切换模型。
4.2 状态定义
我们定义四个主功能状态分数:
其中低 MMP-9 的作用写成去抑制形式:
系统在任一时刻的主状态由得分最高者决定:
我们将系统抽象为五种状态:
其中:
- Repair 表示系统进入抗炎修复模式;
- Anti-PA 表示系统进入铜绿感染响应模式;
- Anti-SA 表示系统进入金葡感染响应模式;
- Exit 表示系统进入安全退出状态。
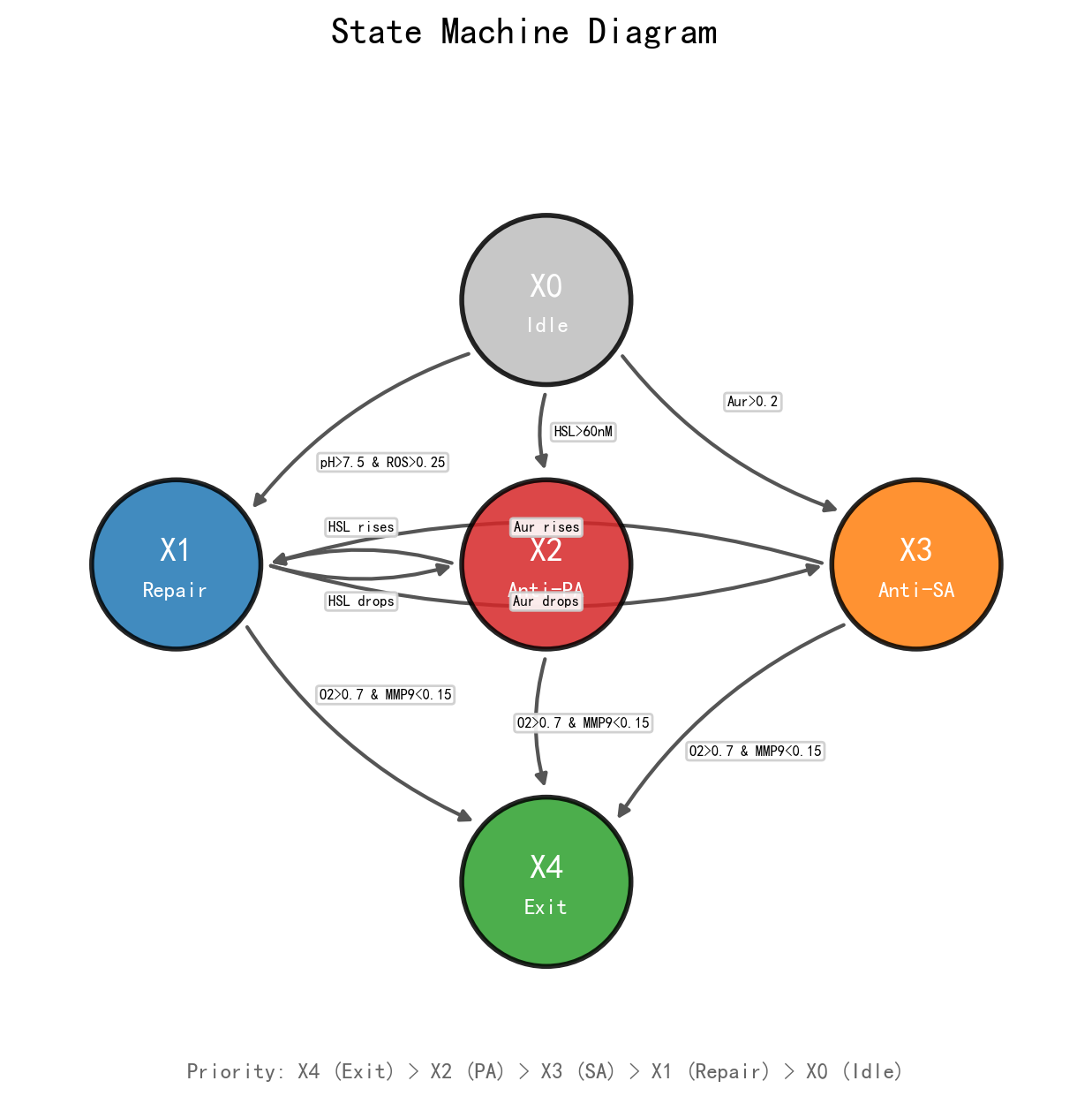
4.3 状态机逻辑
在决策逻辑上,我们设定系统具有明确优先级:
也就是说:
- 一旦满足高氧、低 MMP-9 的愈合后期条件,系统优先进入 Exit;
- 若检测到铜绿感染信号,则进入 Anti-PA;
- 若检测到金葡感染信号,则进入 Anti-SA;
- 否则在高 pH、高 ROS 环境下进入 Repair;
- 若无明显输入,则维持 Idle。
这种状态机逻辑保证了系统在任意时刻只有一个主状态,从而避免多个模块无序竞争。
5. Kill Switch 安全退出模块
5.1 建模目的
对于活体敷料来说,治疗完成后的安全退出同样至关重要。因此我们建立了一个基于 O₂ 与 MMP-9 的 kill switch 模型,用于模拟:
- 高氧激活
- 低 MMP-9 去抑制
- CcdB 表达
- 工程菌数量下降
这一模块的目标是确保工程菌在创面愈合后期能够自动退出,而不会在治疗前期误触发。
kill switch 的核心思想是:
高 O₂ 激活,低 MMP-9 去抑制。
因此我们定义:
因此 kill switch 的总激活强度可表示为:
CcdB 动力学
设 \(CcdB(t)\) 为毒素浓度,则:
工程菌种群变化
设 \(B_e(t)\) 为工程菌数量,则:
其中 \(H(CcdB)\) 为随 CcdB 升高而增强的死亡函数,可用 Hill 形式表示:
该模型描述了工程菌在愈合后期由"存活"向"清除"转变的全过程。
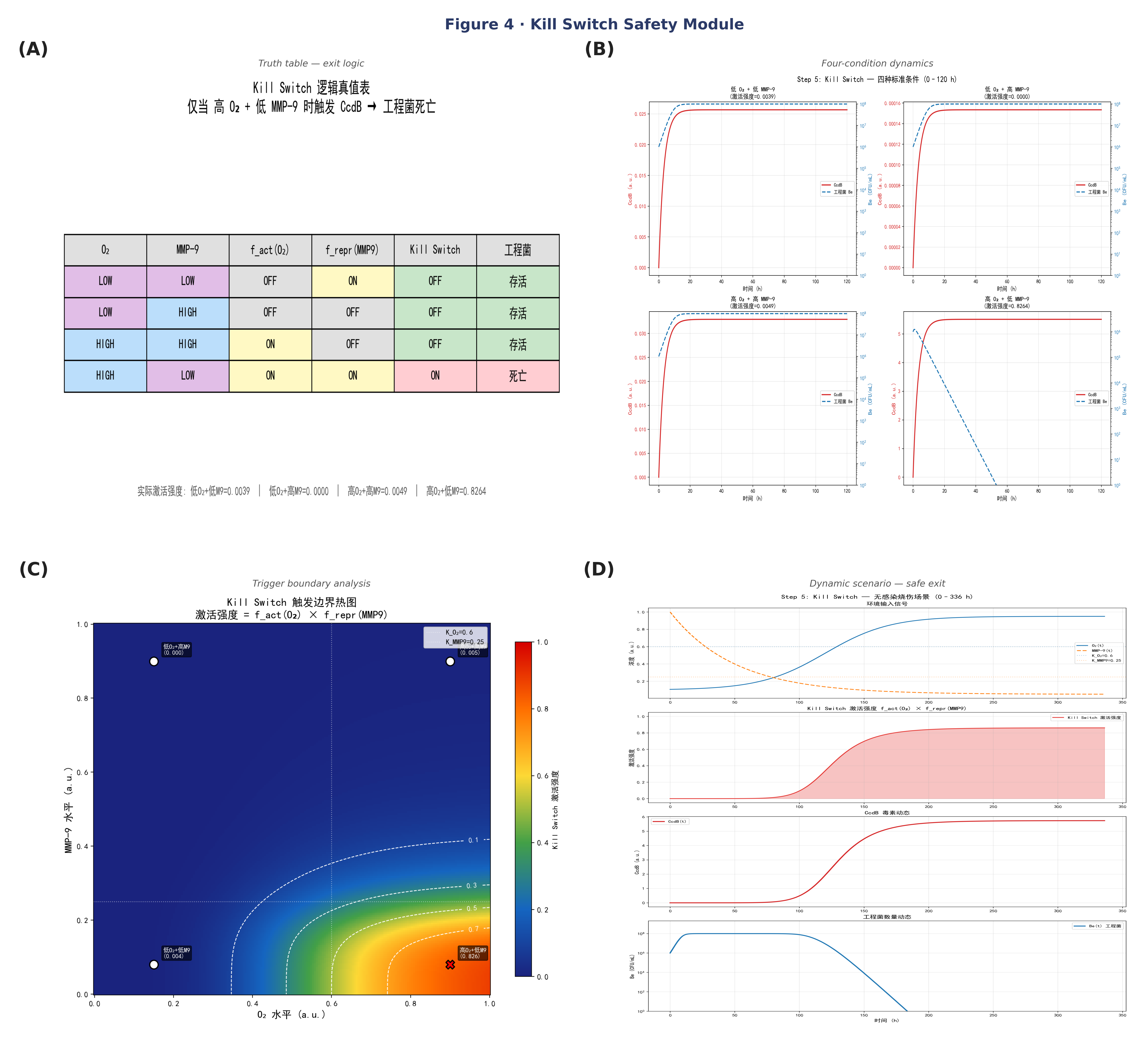
5.2 逻辑与动力学特征
模型结果表明,kill switch 的逻辑条件具有很高的选择性:
- 在三种非触发条件下,系统维持关闭,工程菌存活;
- 在高 O₂、低 MMP-9 条件下,系统被显著激活;
- CcdB 累积后,工程菌数量快速下降。
同时,边界分析表明这一触发过程具有清晰的输入窗口,说明系统既具有较低误触发风险,又能够在愈合后期有效退出。
在无感染场景下,模型进一步表明系统会经历:
这一结果验证了 kill switch 模块在安全性层面的设计目标。
6. 系统级性能评估
6.1 建模目的
在建立了各功能模块和状态切换模型之后,我们进一步构建了系统级性能评估模型,用于回答最终问题:
系统级评估的关键不是单一分子浓度,而是多个功能维度的综合表现。因此我们定义四类系统级指标。
抗炎指数
其中 \(\tilde{S}\) 和 \(\tilde{E}\) 为 SOD、EGF 输出经归一化处理后的指标。
抗菌指数
其中 \(\tilde{B}_{PA}\) 与 \(\tilde{B}_{SA}\) 表示不同感染场景下病原菌清除效果的归一化结果。
修复指数
修复指数反映修复输出与创面修复窗口之间的匹配程度,可表示为:
安全指数
安全指数反映工程菌在后期是否被有效清除:
当最终残留工程菌越低,安全指数越高。
综合评分
最终,我们用加权和表示系统级综合评分:
该评分用于比较主系统、普通敷料和单功能敷料在不同场景下的整体表现。
6.2 对照组设定
为了比较系统级性能,我们设置了两类对照:
普通敷料
- 无环境感知能力
- 无特异性抗菌模块
- 无安全退出机制
单功能敷料
- 仅保留修复模块
- 不具有特异性感染响应
- 不具有 kill switch
通过与这两类对照组比较,可以更清楚地评估多模块协同设计的优势。
6.3 系统级结果
系统级模型整合了:
- 修复模块输出
- 抗感染模块输出
- 工程菌数量变化
- 主状态切换轨迹
- 系统级评分与敏感性分析
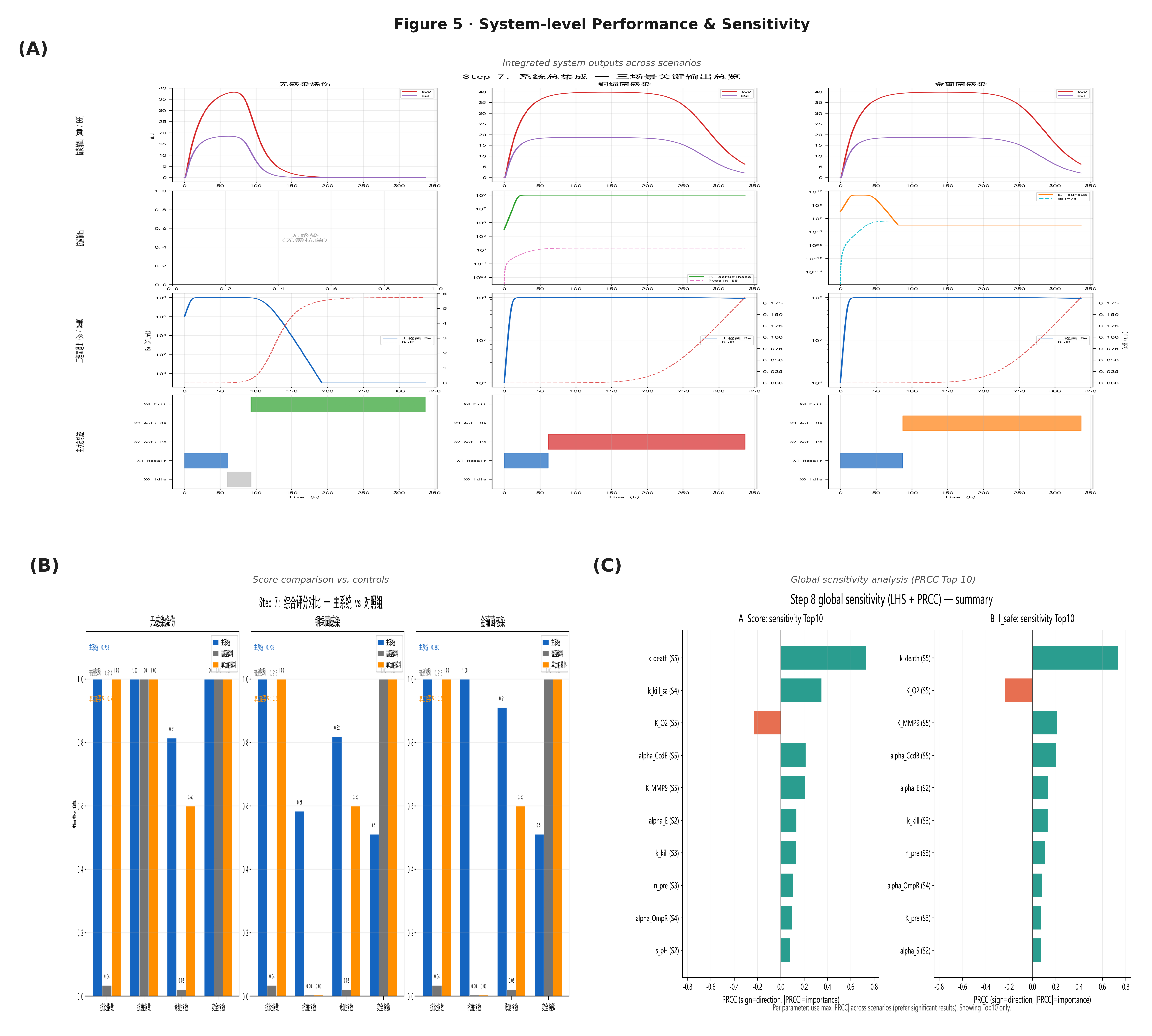
结果表明:
无感染场景
系统主要经历 Repair → Exit,兼具修复与安全清除能力。
铜绿感染场景
系统能够从 Repair 切换至 Anti-PA,说明其具备针对感染的状态转换能力。
金葡感染场景
系统能够从 Repair 切换至 Anti-SA,说明其能够根据不同感染信号进入不同工作模式。
与普通敷料和单功能敷料相比,主系统在多场景下均表现出更好的整体性能,说明本项目的核心优势不在于某一个孤立模块,而在于多模块之间的协调与阶段性切换。
同时,敏感性分析结果进一步指出了最值得优先优化的参数,为后续实验优化提供了方向。
Discussion
本项目的建模并不是为了单纯展示若干拟合曲线,而是为了建立一个能够解释系统行为、预测输出模式并指导后续优化的工程框架。
从当前结果来看,我们的建模支持以下结论:
- 创面环境可以被表示为一组具有阶段性变化的动态输入;
- 抗炎修复模块能够在高 pH 与高 ROS 条件下被准确激活;
- 铜绿响应模块能够识别 HSL 并形成连续输出;
- kill switch 能够在愈合后期实现安全退出;
- 状态机模型表明系统能够根据创面状态进行清晰的主状态切换;
- 系统级模型表明,多模块协同设计优于普通敷料与单功能敷料;
- 敏感性分析指出了后续实验和工程优化最值得优先关注的参数。
因此,这套建模框架证明,本项目并不是单个功能元件的简单组合,而是一个真正的多阶段智能治疗系统。
Conclusion
我们建立了一套完整的烧伤活体敷料建模框架,从创面环境输入出发,逐步描述了抗炎修复、铜绿响应、状态切换、安全退出以及系统级性能。
这些结果表明,本项目的工程菌活体敷料能够根据创面环境的变化,自动完成从早期修复到感染应答,再到后期安全退出的全过程。系统级比较进一步证明,该设计在整体性能上优于传统被动敷料与单功能敷料。
因此,建模不仅验证了设计的可行性,也为后续实验优化和工程迭代提供了明确的定量指导。
参考文献
- [1] Sharpe J R, Booth S, Jubin K, et al. Progression of wound pH during the course of healing in burns[J]. Journal of Burn Care & Research, 2013. PMID: 23128128.
- [2] Ono S, Imai R, Ida Y, et al. Increased wound pH as an indicator of local wound infection in second degree burns[J]. Burns, 2015. PMID: 25468471.
- [3] Parihar A, Parihar M S, Milner S, et al. Oxidative stress and anti-oxidative mobilization in burn injury[J]. Burns, 2008. PMID: 17905515.
- [4] Sharma C, Dobson G P, Davenport L M, et al. The role of matrix metalloproteinase-9 and its inhibitor TIMP-1 in burn injury: a systematic review[J]. 2021. PMID: 34557330.
- [5] Bai Q, Zheng C, et al. Oxygen-releasing hydrogels promote burn healing under hypoxic conditions[J]. Acta Biomaterialia, 2022. PMID: 36210045.
- [6] Weitgasser L, Ihra G, et al. Update on hyperbaric oxygen therapy in burn treatment[J]. 2021. PMID: 31701218.
- [7] Hong W X, Hu M S, et al. The Role of Hypoxia-Inducible Factor in Wound Healing[J]. 2014. PMID: 24804159.
- [8] Struss A K, et al. Toward implementation of quorum sensing autoinducers as biomarkers for infectious disease states[J]. 2013. PMID: 23391272.
- [9] Oscarsson J, Tegmark-Wisell K, Arvidson S. Coordinated and differential control of aureolysin (aur) and serine protease (sspA) transcription in Staphylococcus aureus by sarA, rot and agr (RNAIII)[J]. International Journal of Medical Microbiology, 2006. PMID: 16782403.
- [10] Gustafsson E, Oscarsson J. Maximal transcription of aur (aureolysin) and sspA (serine protease) in Staphylococcus aureus requires sarR activity[J]. 2008. PMID: 18576947.
- [11] Lowy F D. Staphylococcus aureus infections[J]. The New England Journal of Medicine, 1998. PMID: 9709046.
- [12] Church D, Elsayed S, Reid O, et al. Burn wound infections[J]. 2006. PMID: 16614255.
- [13] Kiyohara Y, et al. Cytoprotective effects of epidermal growth factor (EGF) ointment and superoxide dismutase (SOD) ointment on tissue damage at burn sites in rats[J]. 1993. PMID: 8312873.
- [14] Kalay Z, Coskun Cevher S. Oxidant and antioxidant events during epidermal growth factor therapy to cutaneous wound healing in rats[J]. International Wound Journal, 2012. PMID: 22129466.
- [15] Behrens H M, et al. Pyocin S5 Import into Pseudomonas aeruginosa Reveals a Generic Mode of Bacteriocin Transport[J]. mBio, 2020. PMID: 32156826.
- [16] Ling H, Saeidi N, Rasouliha B H, et al. A predicted S-type pyocin shows a bactericidal activity against clinical Pseudomonas aeruginosa isolates through membrane damage[J]. FEBS Letters, 2010. PMID: 20580355.
- [17] Fuchs P C, Barry A L, Brown S D. In vitro antimicrobial activity of MSI-78, a magainin analog[J]. 1998. PMID: 9593152.
- [18] Giacometti A, Cirioni O, Ghiselli R, et al. In vitro activity of MSI-78 alone and in combination with antibiotics against bloodstream isolates[J]. 2005. PMID: 16122911.
- [19] Hallock K J, Lee D K, Ramamoorthy A. MSI-78, an analogue of the magainin antimicrobial peptides, disrupts lipid bilayer structure via positive curvature strain[J]. 2003. PMID: 12719236.
- [20] Bernard P, Couturier M. Cell killing by the F plasmid CcdB protein involves poisoning of DNA-topoisomerase II complexes[J]. Journal of Molecular Biology, 1992, 226(3):735-745. PMID: 1324324.
- [21] Van Melderen L, Bernard P, Couturier M. Lon-dependent proteolysis of CcdA is the key control for activation of CcdB in plasmid-free segregant bacteria[J]. 1994. PMID: 8022284.

