Lab Notebook
本章节详细记录了项目中涉及的所有关键实验,包括质粒设计、启动子筛选、基因沉默评估、OMV检测以及数学建模工作。 每个实验都经过精心设计和验证,以确保结果的可靠性和可重复性。
质粒设计
Plasmid Design & Construction
设计理念
在我们的SynMold系统中,质粒设计是整个项目的基础。我们精心设计并构建了三种关键质粒, 分别用于CRISPR-Cas9基因编辑、dsRNA表达和UV响应自杀系统,以确保系统的高效性和安全性。
pAC-sgRNA-Cas9
CRISPR-Cas9系统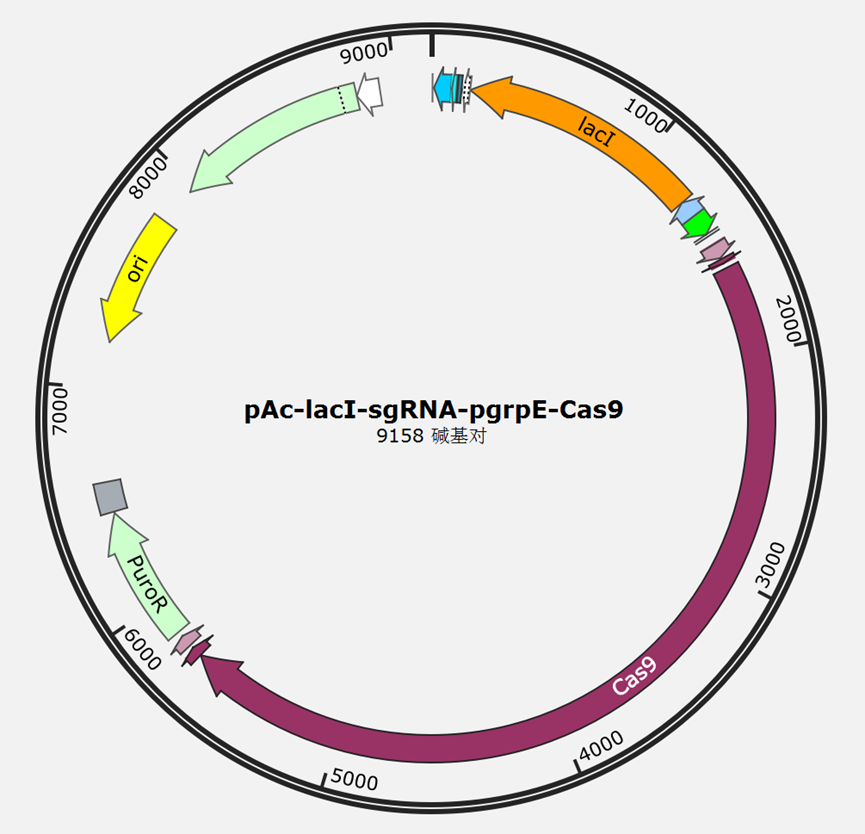
骨架设计
我们决定以SnapGene库中的载体pAC-sgRNA-Cas9作为构建质粒的起点。复制起点为ColE1。此外骨架中还包含lac操纵子序列和PgrpE启动子,用于逻辑门的构建。
选择标记:嘌呤霉素抗性基因作为我们载体原型中的选择标记,支持克隆和实验室测试。
pCDF-dsRNA
dsRNA表达载体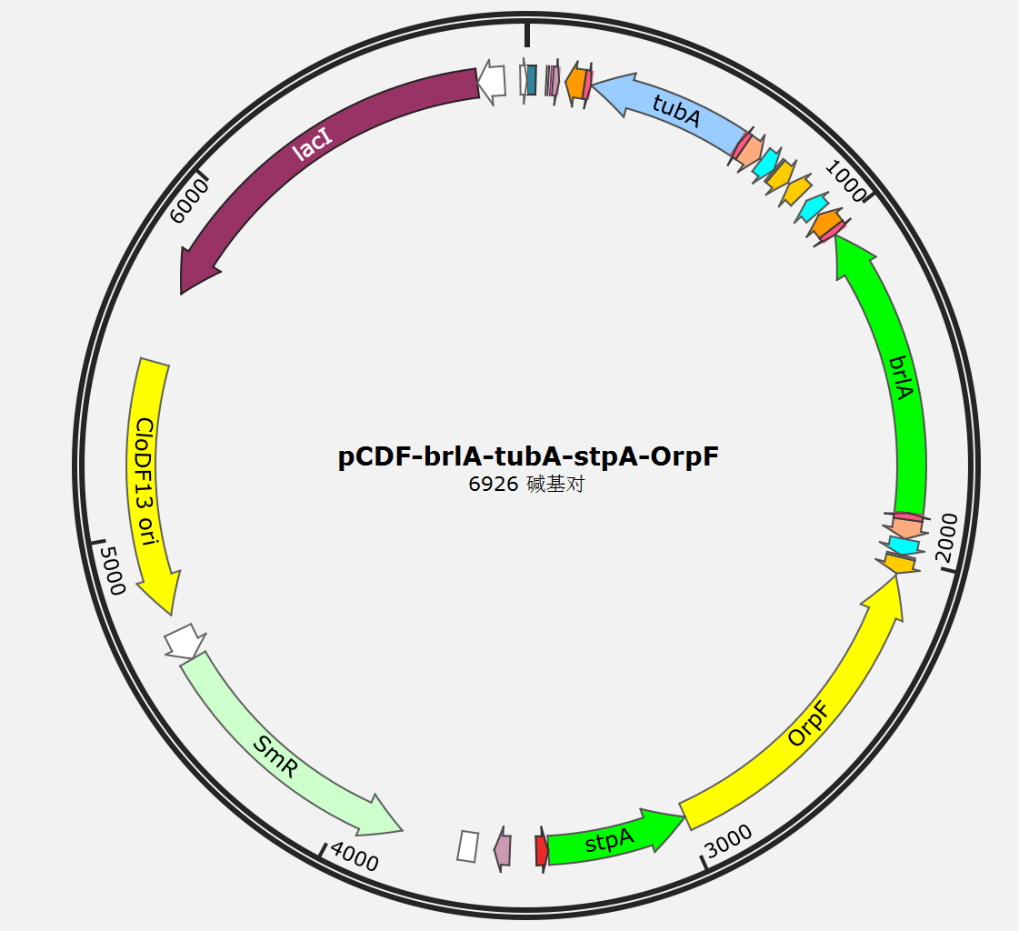
骨架设计
我们决定以SnapGene库中的载体pCDF作为构建质粒的起点。以CloDF13作为复制起点避免了导入质粒间的相互干扰。
dsRNA的表达由两个反向T7启动子控制,与启动子一致,多个T7终止子确保dsRNA生产的停止。
此外在质粒上我们也引入了dsRBD-OrpF蛋白用于在产生dsRNA时辅助锚定。
在选择过程中,我们使用了链霉素抗性基因,该基因已存在于质粒上。
pAC-UV
自杀系统载体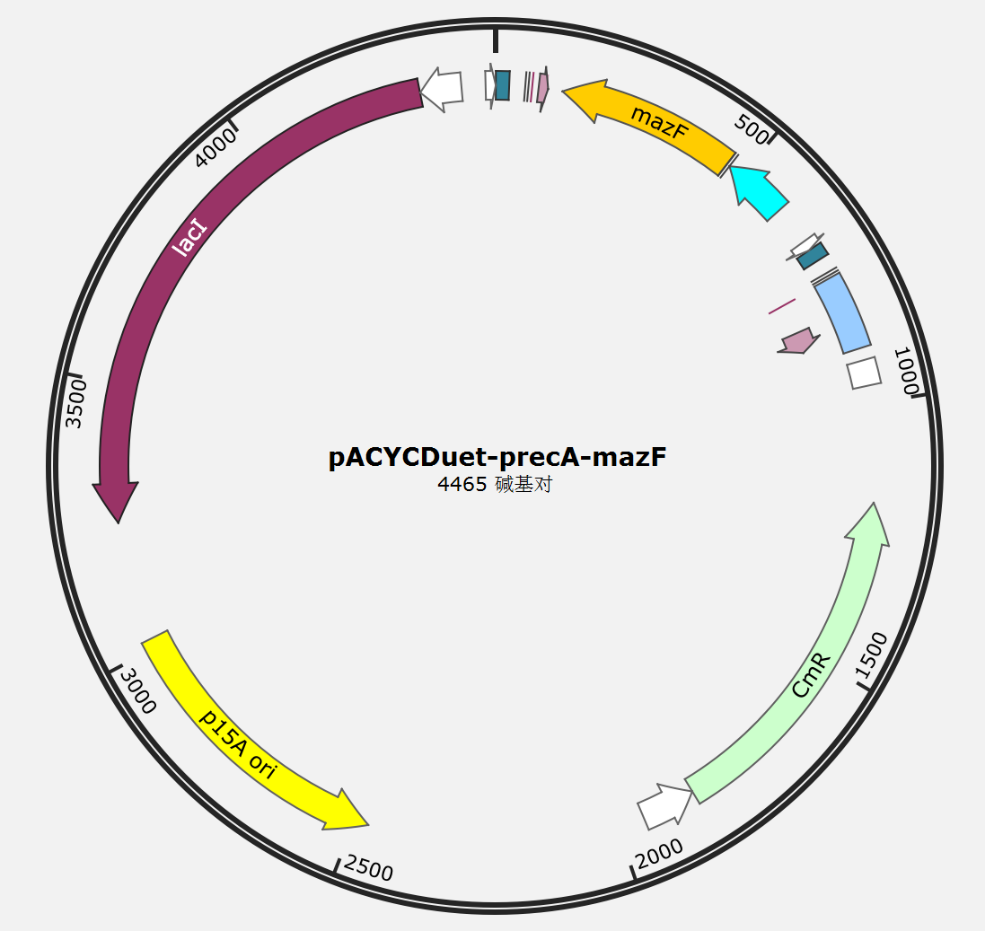
骨架设计
我们决定以SnapGene库中的载体pAC作为构建质粒的起点。以p15A作为复制起点避免了导入质粒间的相互干扰。
该质粒包括了UV启动子、recA以及mazF自杀基因。
利用其上的氯霉素抗性基因进行后续筛选。
T7聚合酶启动子筛选
实验目的
测试并识别调控T7聚合酶的最合适启动子,用于高效生产dsRNA。
实验方法
1. 计算机辅助设计
使用SnapGene软件模拟克隆过程,进行虚拟的琼脂糖凝胶电泳, 以确定用于诊断性消化的最合适的限制酶,并确认条带模式, 从而在进入实验室之前确认最佳的实验流程并确保结果的准确性。
2. 载体构建
将不同的T7启动子克隆到pUPD2载体中。候选启动子包括:
- BG37
- BG42
- BG17
- J23119
- P3.1
- osmY
我们将基本部分从pEGB2载体转移到pDGB3a1和pDGB3a2载体中, 以组装α水平构建体。随后转化到大肠杆菌BL21 DE3细胞中。
3. 菌液培养与诱导
第二天:制备液体培养物以促进转化细菌的生长和适应,37°C温育过夜。
第三天:离心培养物并用NaOH洗涤所得沉淀两次。 稀释至OD600 = 0.4,在37°C诱导6小时。
检测:在酶标仪和荧光倒置显微镜下观察细胞的荧光强度。
预期结果
携带BG37的大肠杆菌在6-12小时仍保持稳定的OD600增长, 进入指数期的时间更长,归一化荧光高。表明:
- 基因表达对细胞的代谢负担更低
- 响应快而且稳定
dsRNA体外沉默评估
实验目的
评估合成的dsRNA对霉菌目标基因的沉默效率,为生物防治应用提供依据。
实验步骤
步骤1:DNA模板创建
使用T7聚合酶创建体外转录所需的DNA模板。 在马铃薯葡萄糖琼脂(PDA)平板上在28°C下培养曲霉, 一旦达到足够的生长,刮取少量菌丝组织并进行RNA提取。
步骤2:RNA提取与纯化
提取RNA后,进行DNase I处理,除去基因组DNA, 确保RNA样品的纯度。然后合成cDNA,作为后续PCR反应的模板。
步骤3:PCR扩增与产物纯化
PCR扩增后,通过凝胶电泳分析PCR产物。 从凝胶上切下正确的条带并纯化。
步骤4:体外转录
利用纯化的DNA模板,进行体外转录步骤以产生dsRNA。
步骤5:96孔板测定
进行96孔板测定来评估dsRNA实施对霉菌的基因沉默效果。 通过测量OD595,每24小时监测真菌的生长,持续10天。
步骤6:RT-qPCR分析
通过RT-qPCR测量相应mRNA的表达水平。 在96孔板中设置四种不同的条件:
- 两种dsRNA处理组
- 孢子组
- 空白对照组
在最后一次OD测量后,在处理组中收集菌丝。 将每组菌丝分成两份,分别放入两个EP管中,作为技术重复, 以提高后续qPCR结果的可靠性。随后进行RT-PCR, 评估dsRNA介导的基因沉默效率。
预期结果
从OD595生长曲线来看,tubA dsRNA处理组表现出:
- 轻微的生长抑制趋势
- 对应的mRNA表达水平下调
VOCs响应启动子筛选
实验目的
筛选能够响应挥发性有机化合物(VOCs)诱导的启动子, 为构建生物传感器奠定基础。
实验方法
1. 菌株活化
将pSB1A3-PgrpE(可替换为PsoxS等多种启动子)-mRFP的 多个报告菌株的甘油菌液划线接种于含100 μg/mL氨苄青霉素的LB琼脂平板上, 37°C培养16小时。
挑取单菌落接种至5 mL含相同抗生素的LB液体培养基中, 37°C、250 rpm振荡过夜培养约16小时。
2. 菌液稀释
将过夜培养物以1:100比例转接至50 mL三角瓶内的10 mL新鲜LB培养基中, 在相同条件下继续培养至OD600 = 0.6 ± 0.05。
3. VOCs处理
将VOCs储备液先用无菌去离子水稀释至0.1%,使用前再稀释1000倍。 在96孔黑色透明底微孔板中:
- 每孔加入90 μL细菌培养液
- 再加入10 μL稀释后的VOCs溶液(终体积100 μL)
- 对照组加入10 μL无菌去离子水
用透气膜封板后,37°C静置孵育4小时。
4. 荧光检测
孵育结束后,将微孔板轻柔振荡10秒:
- 测量OD600,以评估细胞密度
- mRFP荧光在584 nm激发波长和607 nm发射波长下记录
最终测量归一化荧光强度。 使用GraphPad Prism 9.0进行单因素方差分析及Tukey多重比较检验。
预期结果
PgrpE的归一化荧光较高,Fold change > 1,证明:
- 活性上调
- 诱导能力较强
Cas9敲除与OMV检测
实验目的
利用CRISPR/Cas9系统敲除目标基因,并检测外膜囊泡(OMV)的释放情况, 验证基因功能与OMV分泌的关系。
实验方法
1. 菌株准备与活化
将两组菌株进行培养:
- 转染有pAc-sgRNA-cas9质粒的大肠杆菌
- 未处理的野生型大肠杆菌
划线接种于含100 μg/mL氨苄青霉素的LB琼脂平板上,37°C培养16小时。 挑取单菌落接种至5 mL含相同抗生素的LB液体培养基中, 37°C、250 rpm振荡过夜培养约16小时。
2. 大规模培养
将400 mL含抗生素(如需要)的LB培养基预热至37°C, 接种后振荡培养16-20小时。定期测量OD值。
3. OMV分离与纯化
将40-45 mL培养物分装至8个50 mL离心管中。
第一次离心:6000 × g,20分钟,4°C,去除完整细菌细胞。
上清液处理:转入离心管中,再次离心。
第二次离心:100,000 × g,2小时,4°C,沉淀粗OMV。
用PBS重悬沉淀至10 mL,用0.22 μm滤膜过滤, 进一步去除杂质和可能的活菌。
预期结果
离心纯化后有黑色沉淀。
在透射电镜观察下出现球形或类球形囊泡, 即证明该基因的敲除可以增加OMV的产生。
取部分样品分别涂布于LB、LB-amp、LB-kan平板上, 检测是否有活菌污染。
数学建模
建模目标
通过数学建模和生物信息学方法,预测和验证实验结果, 为实验设计提供理论指导。我们的建模工作涵盖细菌生长动力学、 RNA干扰动力学以及RNA-蛋白质互作预测三个主要方向。
1. 细菌生长曲线建模
生长曲线四个阶段
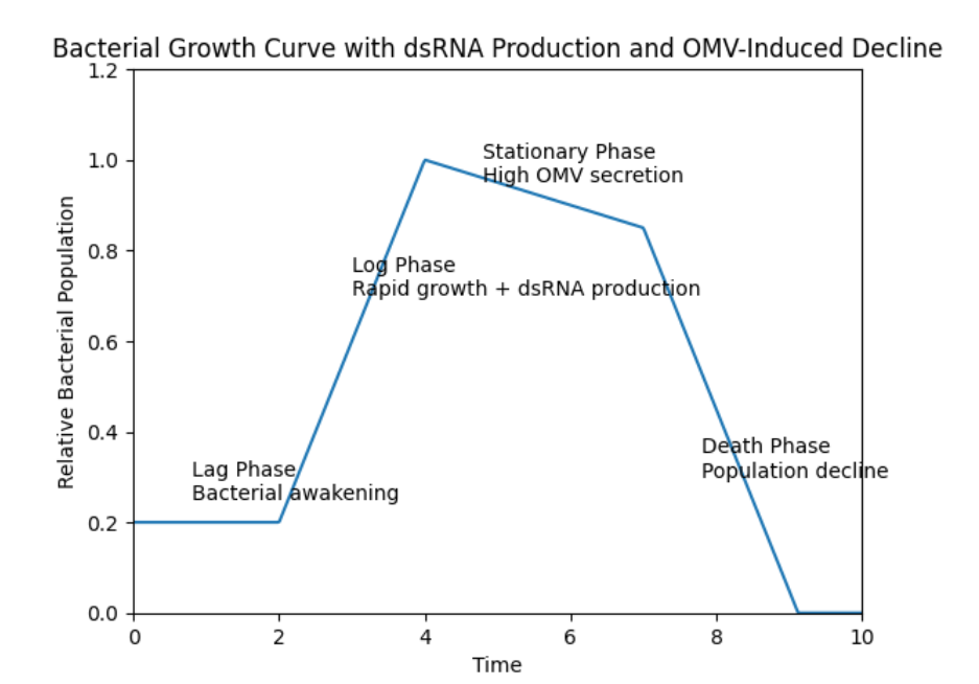
通过常微分方程(ODE)建立细菌生长的动力学模型, 我们将整个生长过程分为四个关键阶段:
- 细菌苏醒阶段:细胞适应环境中,菌体数量基本不变
- 菌群生长期:菌量快速上升至峰值,同时dsRNA开始大量表达
- 静止期:外膜囊泡分泌增强
- 下降期:安全终止阶段,mazF在PrecA下激活
2. RNA干扰动力学建模
ODE方程建模
使用ODE方程建立RNAi作用过程的动力学模型, 利用Python进行图像可视化。该模型描述了mRNA被RNAi降解的时间变化过程。

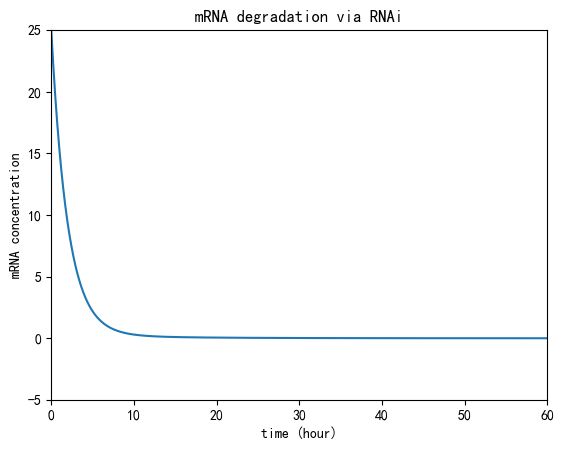
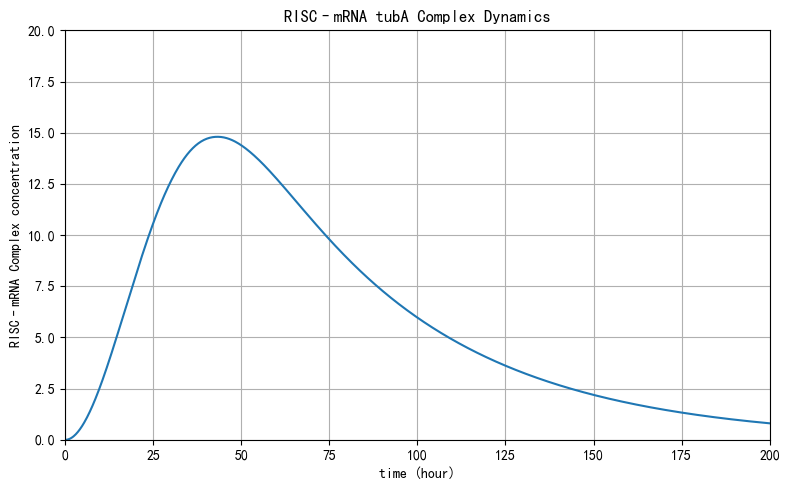
RISC-mRNA复合物动力学
该图描述了RISC–mRNA复合物浓度随时间的变化: 早期RISC与充足的mRNA结合形成复合物,随后mRNA被持续消耗导致底物限制, 使复合物生成速率下降并最终衰减。
RNAi机制简介:RNAi(RNA interference)是一种由双链RNA(dsRNA)触发的 序列特异性基因沉默机制:
- 长dsRNA在细胞内被RNase III家族酶Dicer切割成约21-23 nt的小干扰RNA(siRNA)
- siRNA被加载到Argonaute蛋白上,去除其中一条链后形成成熟的RNA-诱导沉默复合物(RISC)
- RISC依靠保留的向导链与靶mRNA互补配对,在高度互补的情况下由Argonaute催化切割靶mRNA
- 靶mRNA被降解,从而抑制相应蛋白的表达
3. RNA二级结构预测
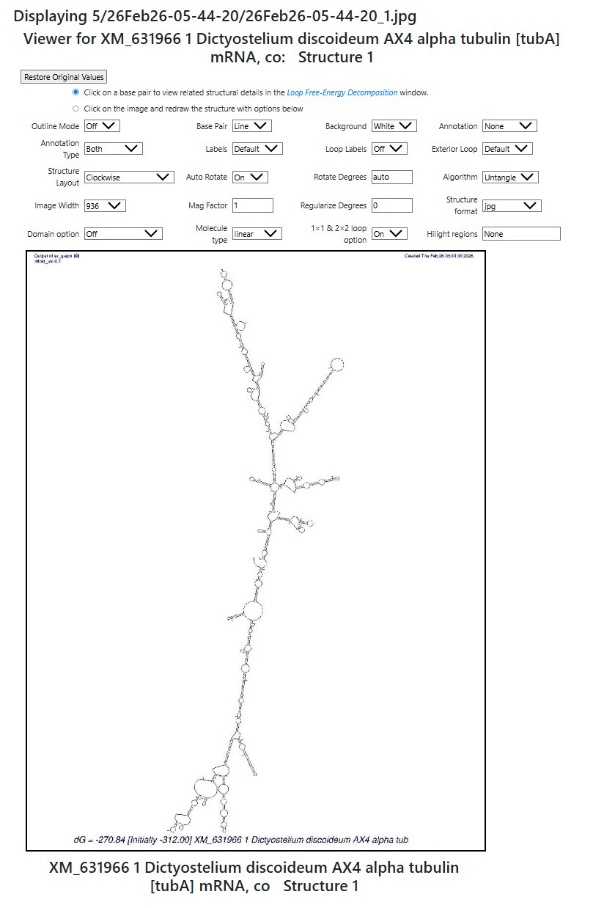
利用RNAfold进行二级结构建模
首先利用RNAfold对tubA的二级结构进行建模, 验证dsRNA和dsRBD的结合效力,此处以tubA为例。 然后利用AlphaFold3对tubA进行三维结构的观测以及与stpA结合力的检测。
4. RNA-蛋白质互作预测
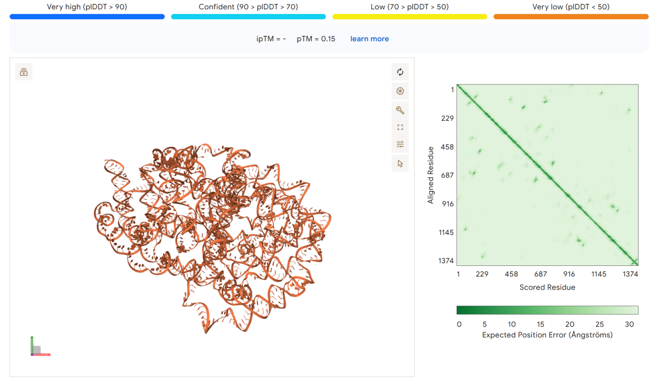
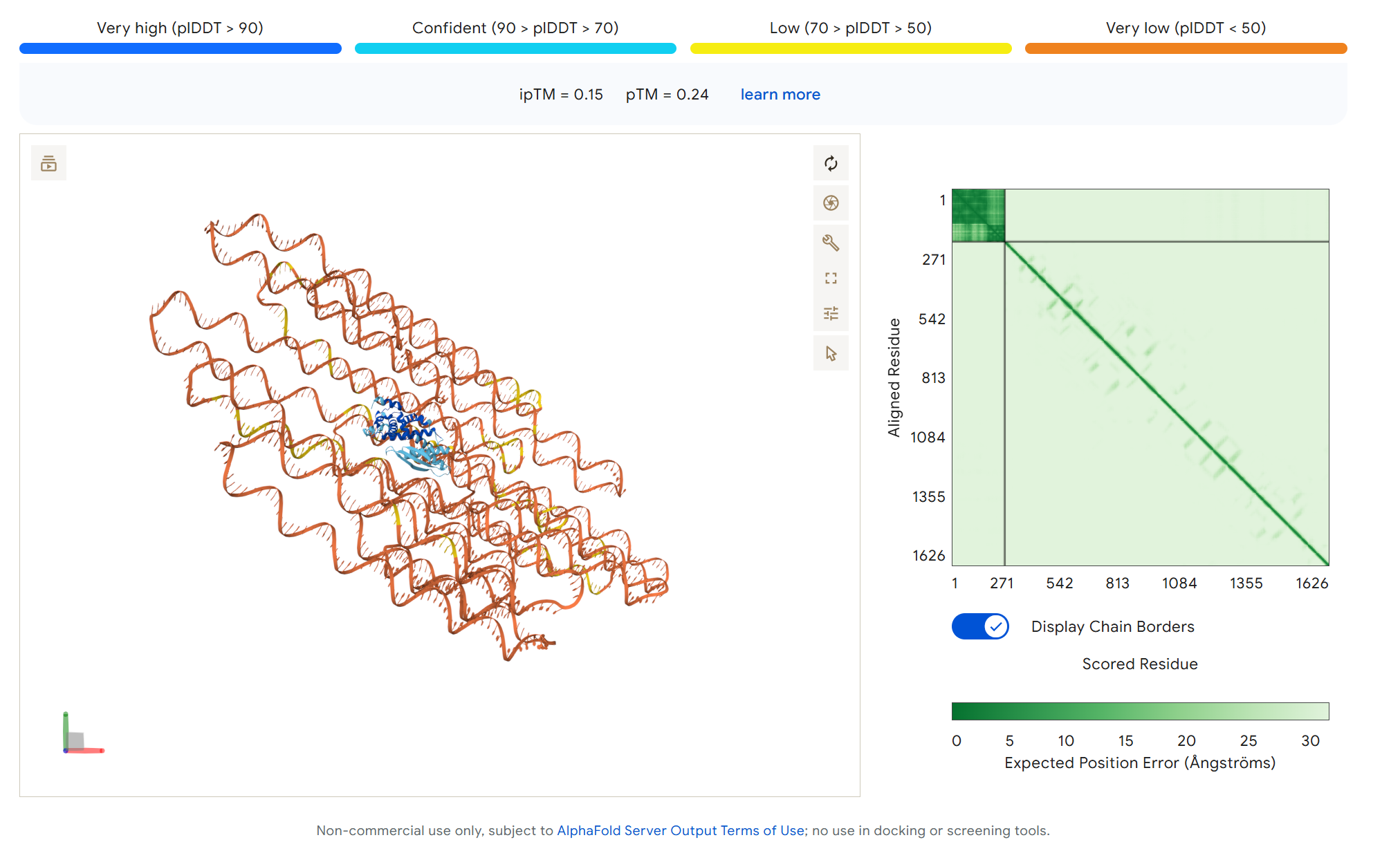
AlphaFold3三维结构预测
利用AlphaFold3预测tubA与stpA蛋白的结合情况。 初步结果显示dsRNA和dsRBD的结合并不理想,原因可能包括:
- dsRNA基因序列太长
- stpA蛋白性能不佳,包含大量无序区域
改进方案
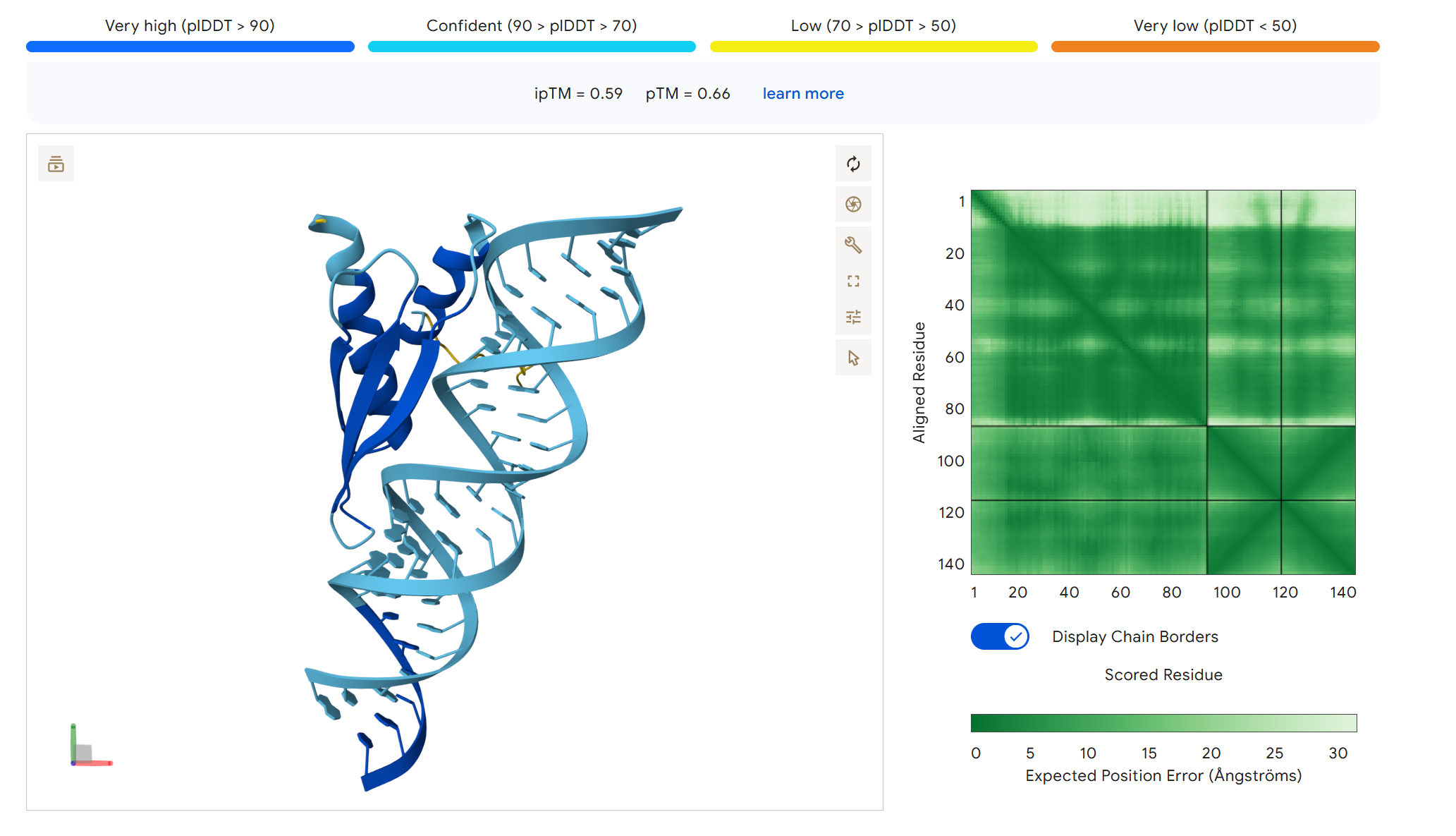
针对初步预测结果不理想的问题,我们提出以下改进方案:
- 更换dsRBD:选择RNase Ⅲ作为一种天然的RNA酶, 但只保留其中的RNA结合结构域(dsRBD)
- 截取有效片段:选择只截取tubA部分有效片段, 减少off-target风险,同时避免包含与其他基因相似的保守区域
结果:可见模块简化后预测置信度显著提升,证明了该方案的可行性。
5. PyMOL结构分析
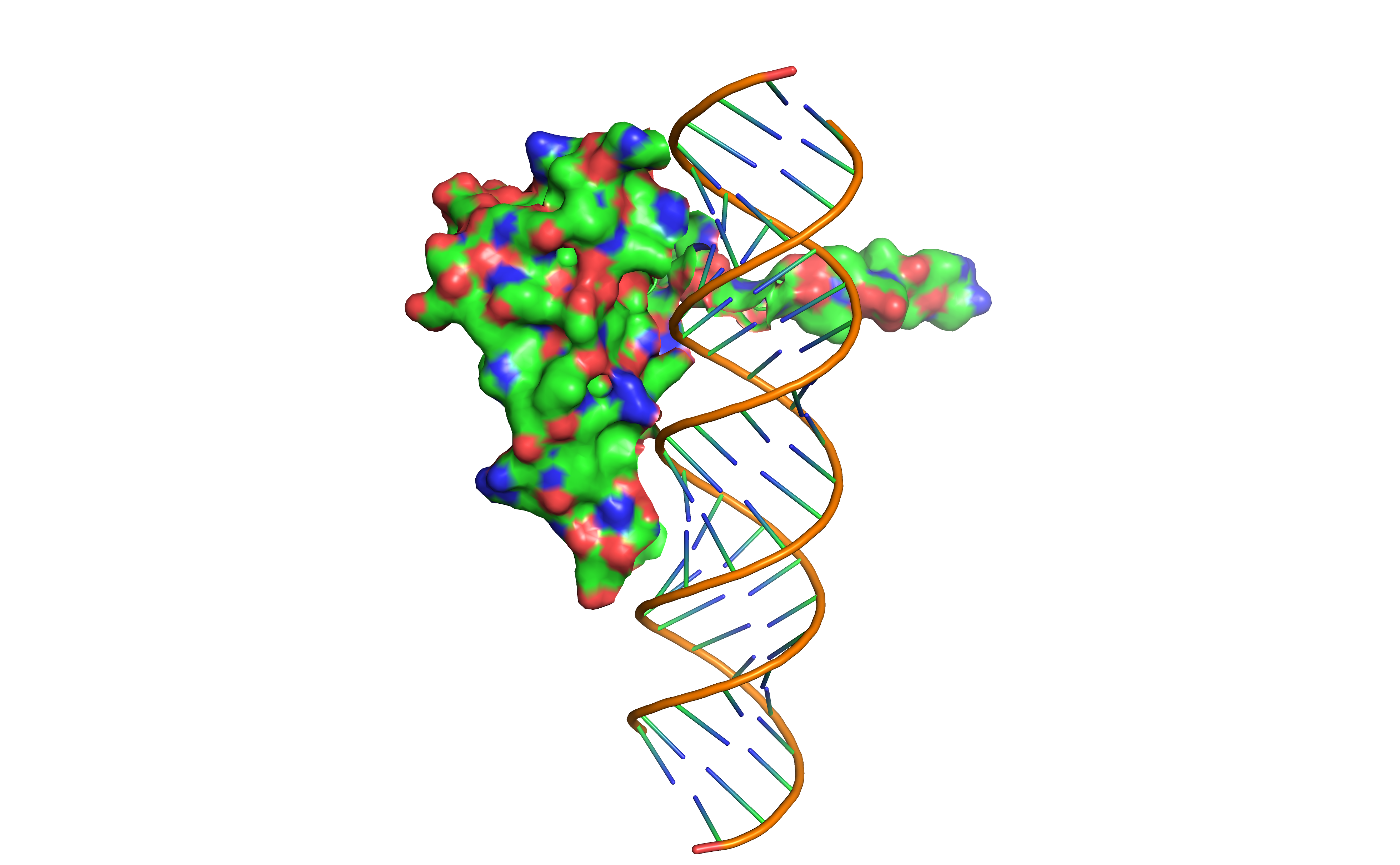
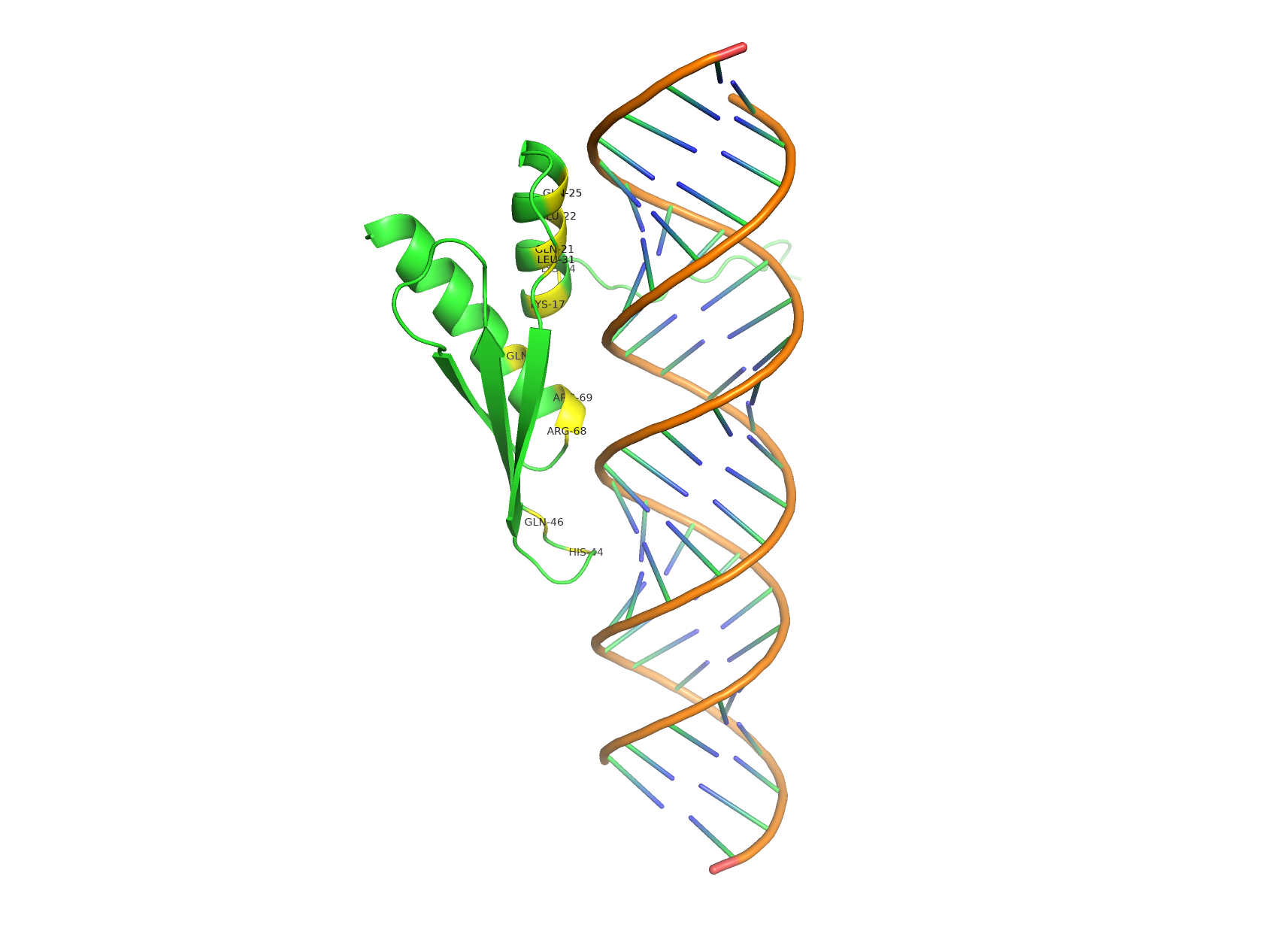
三维结构详细分析
后续利用PyMOL软件分析了model0构象,显露了其中具体的结合位点, 为实验设计提供了精确的结构信息。
建模总结
通过多层次的数学建模和生物信息学分析,我们:
- 建立了完整的细菌生长动力学模型,指导实验时间设计
- 通过RNAi动力学建模,优化了dsRNA的作用策略
- 利用RNAfold和AlphaFold3预测了RNA结构和蛋白质互作
- 通过PyMOL深入分析了结合位点,为实验改进提供了理论依据
这些建模工作不仅帮助我们理解了系统的动力学特性, 还为后续实验设计提供了重要的理论指导。