实验设计
实验针对肠道靶向除臭工程菌开展系统性验证,从功能实现、节律调控、生物安全三方面搭建完整实验体系。
一、核心除臭模块
验证思路:采用「表面展示→调控表达→结合前体→屏障拦截」四步递进验证思路,系统拆解除臭功能的实现路径。
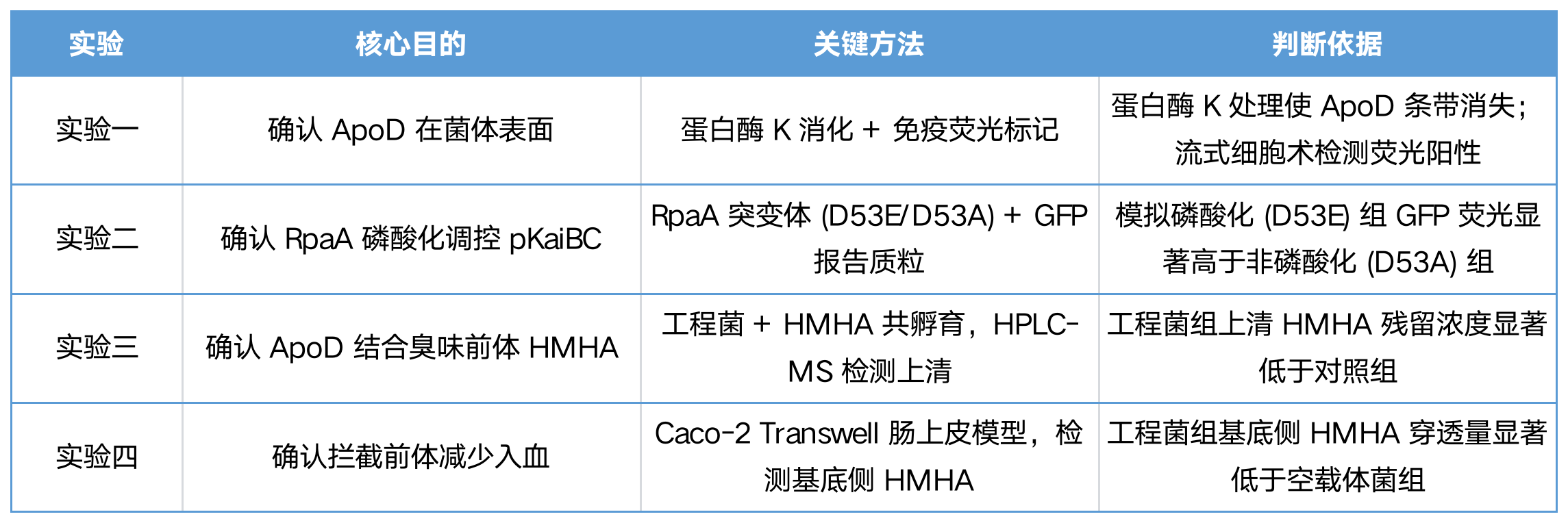
步骤 1(表面展示验证)
实验方法:首先通过蛋白酶 K 消化联合免疫荧光标记实验,验证 ApoD 蛋白成功锚定在菌体表面。
预期结果:蛋白酶 K 处理可使 ApoD 条带消失,流式细胞术检测呈现荧光阳性。
步骤 2(调控表达验证)
实验方法:进一步利用 RpaA 磷酸化突变体 (D53E/D53A) 结合 GFP 报告质粒,证实 KaiBC 节律系统对功能蛋白的精准调控。
预期结果:模拟磷酸化的 D53E 组 GFP 荧光信号显著高于非磷酸化的 D53A 组。
步骤 3(结合前体验证)
实验方法:随后通过工程菌与臭味前体 HMHA 共孵育,结合 HPLC-MS 技术检测上清液,确认工程菌可高效结合并清除 HMHA。
预期结果:工程菌组上清中 HMHA 残留浓度显著低于对照组。
步骤 4(屏障拦截验证)
实验方法:最后借助 Caco-2 Transwell 肠上皮模型模拟肠道屏障环境,检测基底侧 HMHA 含量。
预期结果:证明工程菌能显著拦截前体分子穿透肠屏障,有效减少其入血风险,从源头实现除臭目标。
二、昼夜节律调控模块
验证体系:构建「体外重构→体内报告→通路验证」的三级验证体系,全面解析节律系统的功能与调控机制。
步骤 1(体外层面验证)
实验方法:体外层面,重构 KaiABC 蛋白与 ATP 反应体系,通过 Phos-tag 电泳技术。
预期结果:确认 KaiC 蛋白磷酸化水平呈现 24 小时自主振荡规律。
步骤 2(体内层面验证)
实验方法:体内层面,将三质粒共转化至大肠杆菌,经阿拉伯糖诱导后实时监测荧光信号。
预期结果:验证节律输出的稳定性与人为可调可控性。
步骤 3(通路层面验证)
实验方法:通路层面,构建 △SasA/RpaA 基因缺失株,通过检测报告基因表达及 RpaA 磷酸化水平。
预期结果:明确 SasA/RpaA 是连接核心节律振荡与下游功能蛋白表达的关键信号通路,保障功能输出的节律性。
三、生物安全模块
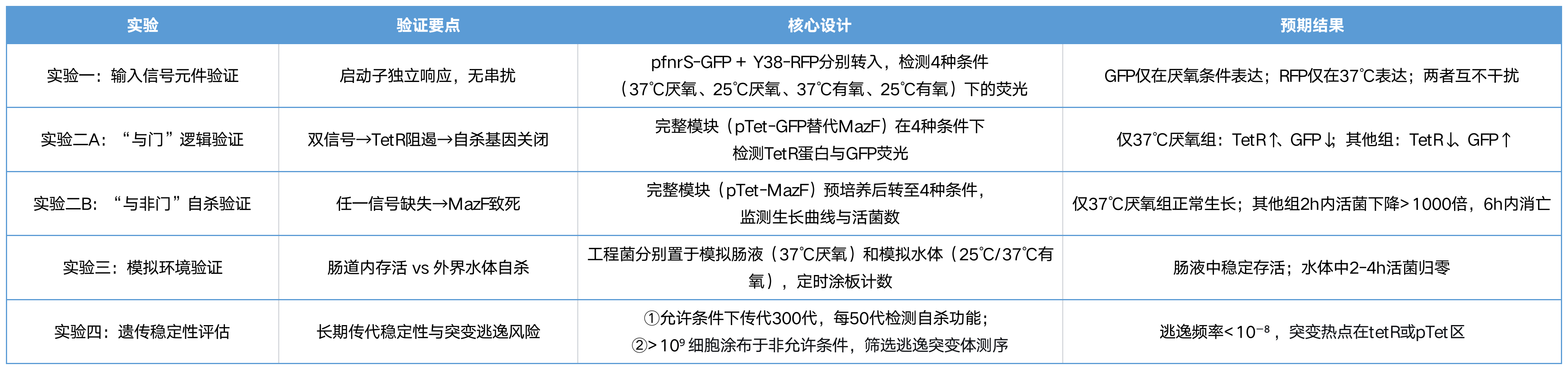
设计理念:基于缺氧与 37℃ 双信号驱动的「与非门」逻辑,搭载 MazF 自杀基因,通过多维度实验严格验证环境安全性。
步骤 1(输入信号元件独立性验证)
实验方法:首先验证输入信号元件的独立性。
预期结果:pfnrS-GFP 与 Y38-RFP 分别响应缺氧与 37℃ 信号,两者表达互不干扰。
步骤 2(「与门」逻辑严谨性验证)
实验方法:随后验证「与门」逻辑的严谨性。
预期结果:双信号存在时 TetR 阻遏自杀基因,仅 37℃ 厌氧环境下 TetR 高表达、GFP 低表达,其他条件下则相反。
步骤 3(「与非门」自杀验证)
实验方法:进一步通过「与非门」自杀验证。
预期结果:确认仅在肠道模拟环境 (37℃ 厌氧) 中工程菌可正常生长,脱离该环境后 2 小时内活菌数下降超 1000 倍,6 小时内近乎消亡。
步骤 4(模拟环境与稳定性实验)
模拟环境实验结果:证实工程菌在模拟肠液中稳定存活,在模拟水体中 2-4 小时内活菌归零。
长期遗传稳定性评估结果:显示,工程菌逃逸频率低于 10⁻⁸,突变热点集中于 tetR 或 pTet 区域,无环境扩散风险,符合严格的生物安全标准。