人类实践
一、项目背景
狐臭作为由 ABCC11 基因突变驱动的常见体表问题,其核心病理机制为顶泌汗腺分泌的无臭前体经皮肤菌群分解产生异味羧酸,不仅造成生理困扰,更对患者心理健康与社会交往形成显著影响。调研数据显示,狐臭是导致大学生自卑、焦虑及社交障碍的重要诱因,超 80% 的患者存在心理负担加重、社交回避等表现,部分患者因担心遗传而放弃生育,或因体味问题遭受校园霸凌与职场歧视。现有治疗手段的局限性与患者对安全、长效方案的迫切需求,凸显了研发新型干预策略的必要性与紧迫性。
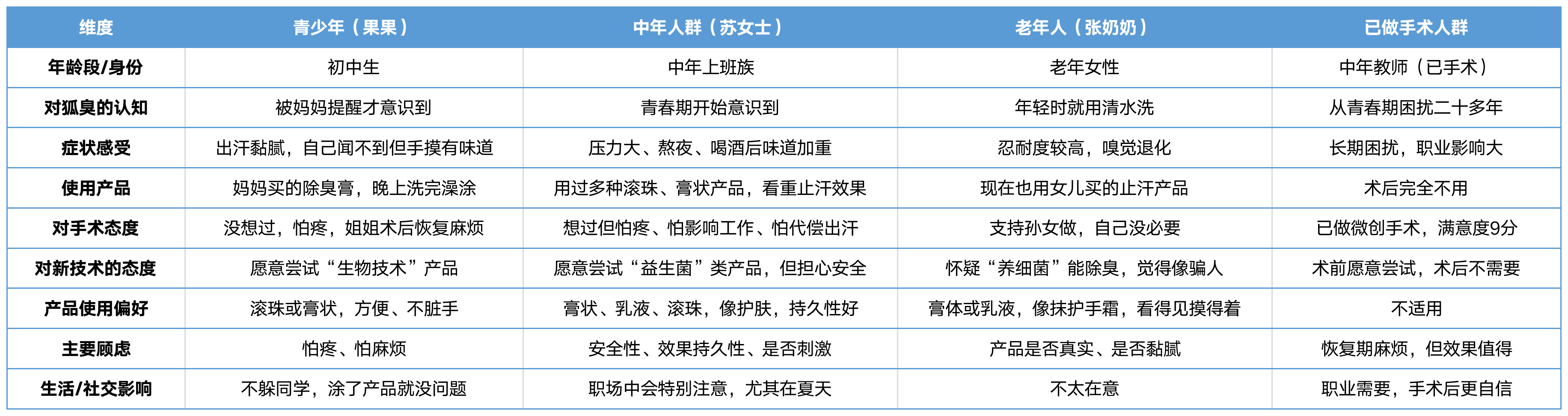
二、前期调研
当前狐臭干预手段主要分为外用药物、微创治疗与手术治疗三类,但均存在难以兼顾疗效、安全性与便捷性的核心缺陷。外用除臭剂与止汗剂仅能临时遮盖气味或抑制汗液分泌,无法阻断前体转运与细菌分解的核心环节,且长期使用易引发皮肤干燥、色素沉着或过敏反应;光电、注射等微创治疗虽可精准破坏顶泌汗腺,但疗效维持时间短(3-6 个月)、治疗成本高,需多次干预;手术切除虽能实现根治,但存在有创留疤、恢复期长及皮瓣坏死、感染等并发症风险,且部分患者术后仍存在复发可能。整体而言,现有方案未能满足「疗效持久、无创便捷、安全可控」的临床需求,存在显著的技术空白。

三、初步设想
基于狐臭的病理机制,项目初期提出外用工程菌干预策略:构建兼具功能模块与安全模块的大肠杆菌工程菌,功能模块通过分泌功能蛋白实现双重作用——降解已生成的臭味分子、抑制腋下产臭菌活性;安全模块搭载阿拉伯糖诱导的 araBAD 启动子调控致死 E 蛋白表达,可通过外源添加阿拉伯糖触发工程菌自杀,实现人工可控的生物安全保障。该方案旨在通过局部外用重塑腋下微生态,在不破坏皮肤正常生理功能的前提下干预狐臭产生。
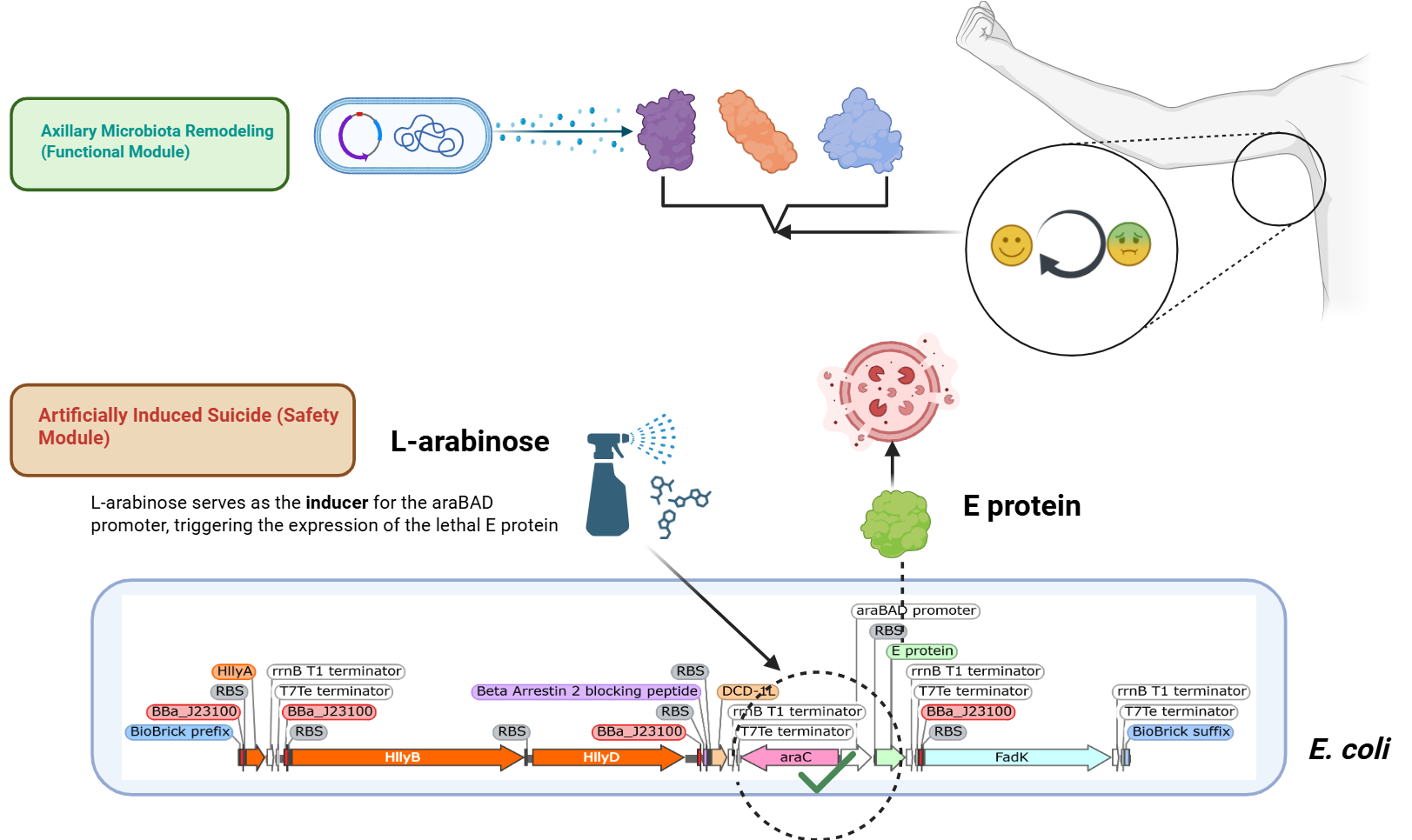
初步设想示意图
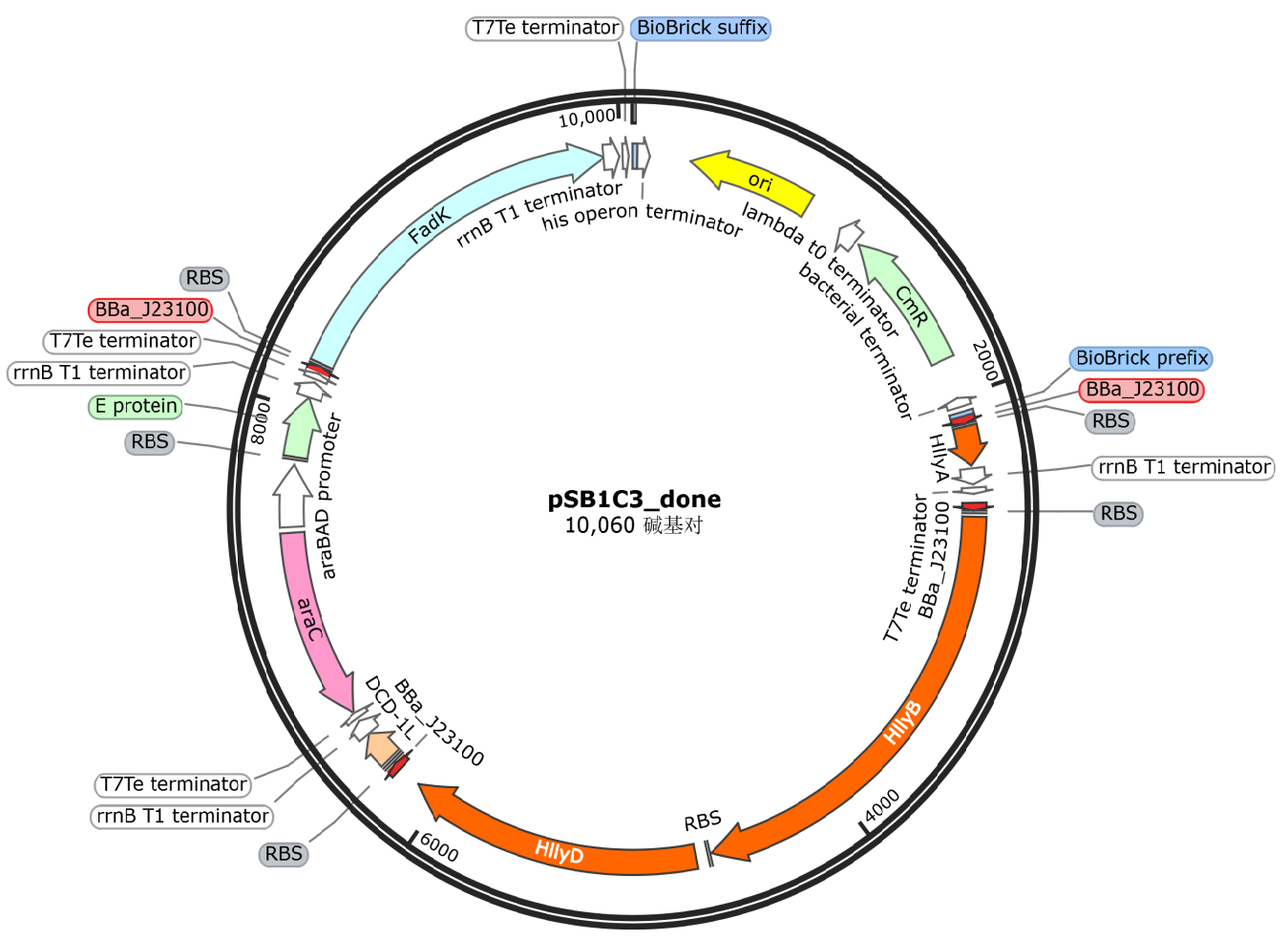
质粒
四、反思调整
1、初始外用方案调研反馈
用户对「可诱导失效」的安全设计认可度较高,认为该设计有效提升了产品使用安全感;但核心反馈指出,外用工程菌模式与市售除臭产品无本质差异,且需搭配阿拉伯糖诱导剂使用,反而增加了操作复杂度,同时用户更倾向于膏状、乳液状等贴近日常护肤习惯的便捷剂型。
2、市售外用产品的核心局限
各类外用除臭产品均无法实现根源干预,仅能临时遮盖气味或抑制汗液分泌,长期使用易引发皮肤干燥、过敏、色素沉着等不良反应;医疗级外用产品虽效果更显著,但存在疗效维持时间短、需多次干预或潜在皮肤刺激等问题,难以满足长效、安全的需求。
3、内服药物路径的科学障碍
狐臭病理靶点为顶泌汗腺,与消化系统无直接通路,口服药物难以精准靶向、易产生全身副作用;抑制汗腺类药物获益有限,长期使用风险超过体味困扰本身;口服抗生素虽可暂时抑制产臭菌,但会破坏肠道菌群平衡并诱导耐药,不适合长期使用。
4、最终方案迭代方向
基于上述反思,项目转向口服、肠道靶向工程菌策略:在臭味前体入血前于肠道内实现拦截,实现源头除臭;同时引入昼夜节律调控模块实现功能分时表达,并建立肠道特异性生物安全模块,确保工程菌仅在肠道环境中存活,有效弥补现有方案「疗效短、有创、不便」的核心短板。

五、工程循环
第一轮循环
设计:设计三功能协同模块,构建质粒,验证酶活性。
反思:当前外用方案与市售产品同质化、使用不便;转向口服、肠道靶向思路。
第二轮循环
设计:引入 KaiABC 生物钟实现昼夜节律调控,构建信号转导通路,验证 24 小时节律输出。
反思:肠道定植、安全性、模块正交性等问题待解决。
第三轮循环
设计:设计表面展示与双输入安全模块,构建融合蛋白,验证前体结合效率。
反思:优化 ApoD 亲和力可进一步提升捕获效率至 90% 以上。
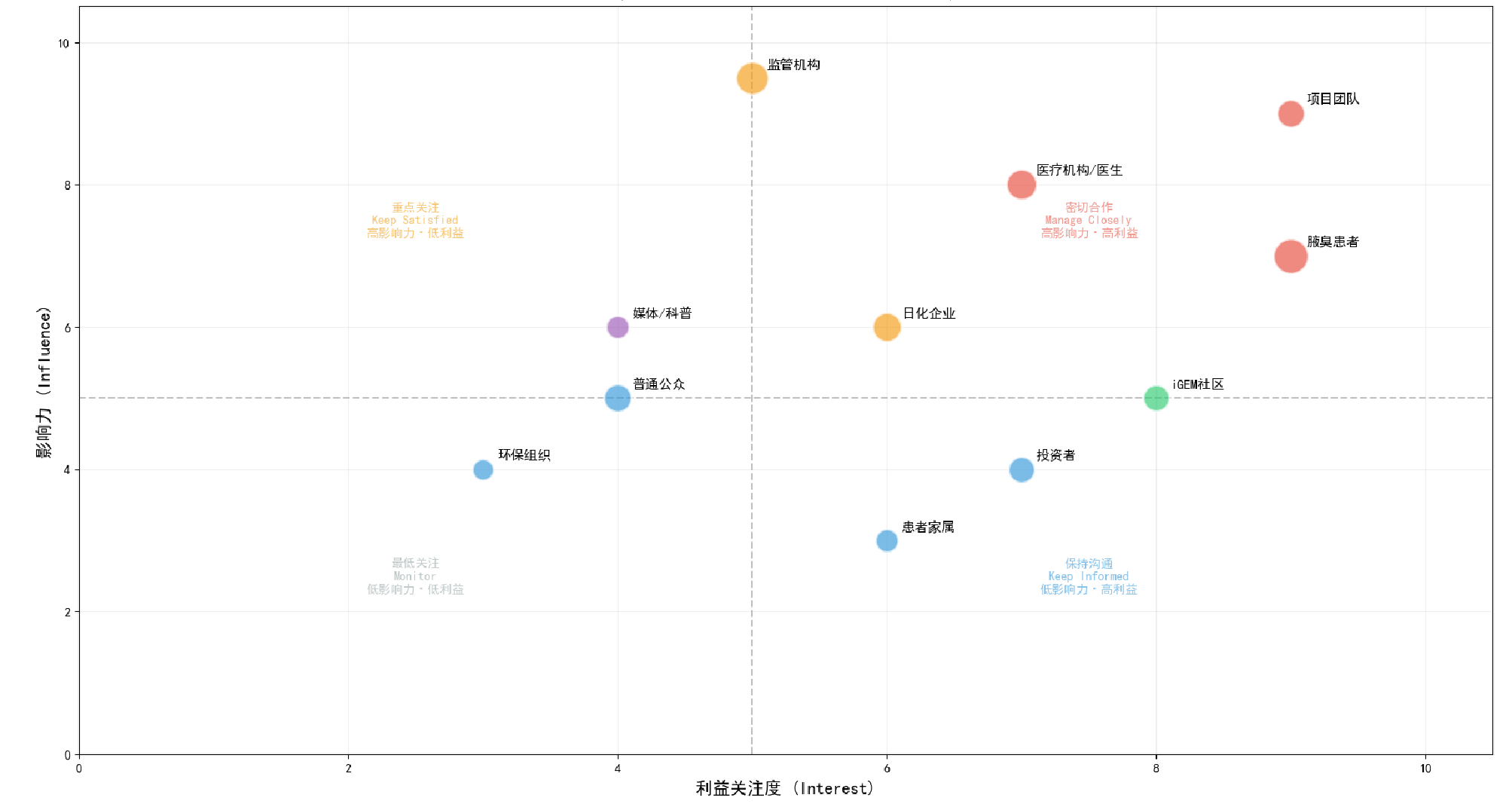
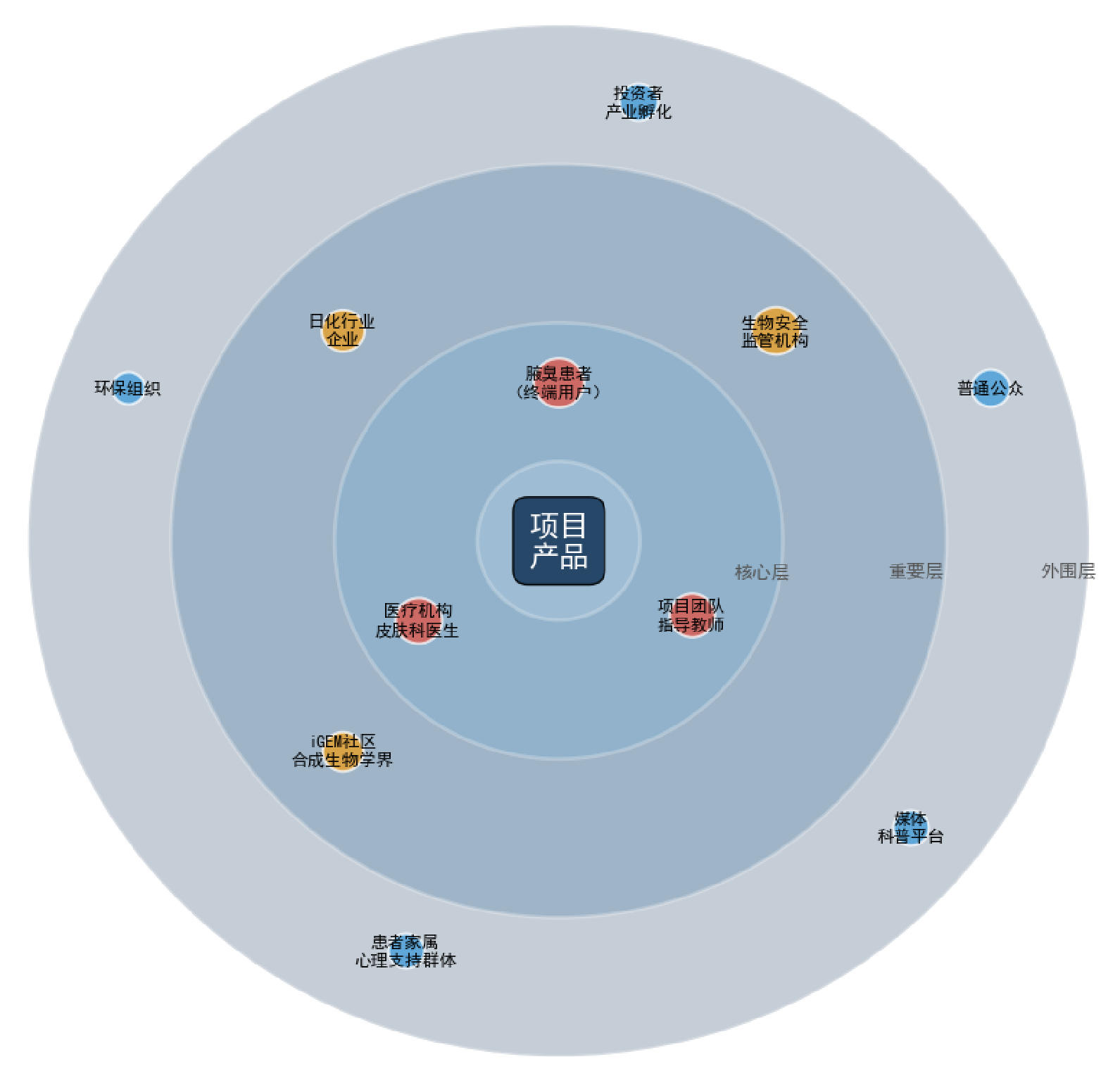
六、利益相关者分析
核心层包括腋臭患者(终端受益)、医疗机构/医生(影响可信度)、项目团队/导师(决定项目质量);重要层包括生物安全监管机构(决定上市)、日化企业(市场合作/竞争)、iGEM/合成生物学社区(技术支持);外围层包括普通公众(舆论导向)、投资者/孵化器(商业化资源)、环保组织(生态关注)、患者家属(心理支持)。
七、SWOT 分析
优势 (S)
- 患者需求迫切、群体基数大
- 项目技术原创(长效、无创、节律调控)
- 日化渠道成熟、公众健康意识提升
劣势 (W)
- 用户对工程菌认知门槛高
- 不同年龄层需求差异大
- 长期安全数据待补充、生产工艺复杂
机会 (O)
- 现有方案痛点显著
- 政策关注心理健康
- 合成生物学与个性化医疗趋势利好
威胁 (T)
- 公众对生物制品安全存疑
- 监管不确定性
- 竞品价格优势与传统诊疗惯性